Diidrofolato reduttasi
La diidrofolato reduttasi (DHFR) è un enzima che catalizza la riduzione dell'acido diidrofolico ad acido tetraidrofolico, con l'utilizzo di NADPH come donatore di elettroni, secondo la seguente reazione:
| diidrofolato reduttasi | |
|---|---|
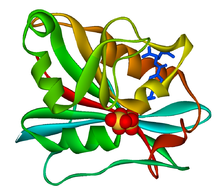 La diidrofolato reduttasi umana in complesso con una molecola di acido folico (viola). In verde il NADPH. | |
| Numero EC | 1.5.1.3 |
| Classe | Ossidoreduttasi |
| Nome sistematico | |
| 5,6,7,8-tetraidrofolato :NADP+ ossidoreduttasi | |
| Altri nomi | |
| tetraidrofolato deidrogenasi; DHFR; acido folico reduttasi; NADPH-diidrofolato reduttasi | |
| Banche dati | BRENDA, EXPASY, GTD, PDB (RCSB PDB PDBe PDBj PDBsum) |
| Fonte: IUBMB | |
| Diidrofolato reduttasi | |
|---|---|
| Gene | |
| HUGO | DHFR |
| Locus | Chr. 5 q11.2-q13.2 |
| Proteina | |
| UniProt | P00374 |
| PDB | 7DFR |
- 5,6,7,8-tetraidrofolato + NADP+ ⇄ 7,8-diidrofolato + NADPH + H+
Nella forma presente negli animali e in alcuni microrganismi, l'enzima è anche in grado di ridurre (con una velocità ridotta) il folato a 5,6,7,8-tetraidrofolato.
Importanza clinica modifica
Dal momento che il tetraidrofolato, prodotto della reazione, è la forma attiva dell'acido folico nell'uomo, l'inibizione della DHFR può causare un deficit funzionale di acido folico. Dal momento che esso è necessario alle cellule a rapida proliferazione per la produzione di timina, questo effetto può essere terapeutico.
Il metotrexato è l'inibitore più importante della DHFR, in grado di legare l'enzima con una affinità 1.000 volte maggiore di quella dell'acido folico. Assieme all'aminopterina è stato il primo anti-folico a trovare impiego come chemioterapico, perché in grado di bloccare la crescita incontrollata delle cellule tumorali.
Divenne subito la prima arma di battaglia contro le leucemie infantili assieme allo steroide prednisone, associazione che permetteva di ottenere prolungate remissioni cliniche.[1] Oggi si usa soprattutto nelle leucemie e nei linfomi, ma altri tumori come osteosarcoma, sarcoma di Ewing, il corioncarcioma, il carcinoma renale e polmonare, comprendono nella loro batteria di farmaci anche il metotrexato (per approfondimenti vedere alla voce antineoplastici)
Altre molecole che agiscono sulla DHFR sono ad esempio gli antimalarici pirimetamina e il proguanile, l'antifolico trimetoprim, molto noto perché associato ad un sulfamidico, il sulfametoxazolo, in commercio col nome di Bactrim.
Note modifica
- ^ (EN) Pooja Chawla, Ghanshyam Teli, Rupinder Kaur Gill e Raj Kumar Narang, An Insight into Synthetic Strategies and Recent Developments of Dihydrofolate Reductase Inhibitors, in Chemistry Europe, vol. 6, n. 43, 18 novembre 2021, pp. 12101-12145, DOI:10.1002/slct.202102555.
Bibliografia modifica
- (EN) R.L. Blakley e B.M. MacDougall, Dihydrofolic reductase from Streptococcus faecalis, vol. 241, n. 13, R. J. Biol. Chem., 1961.
- Bolin, J.T., Filman, D.J., Matthews, D.A. e Kraut, J. Crystal structures of Escherichia coli and Lactobacillus casei dihydrofolate reductase refined at 1.7 Å resolution. I. General features and binding of methotrexate. J. Biol. Chem. 257 (1982) 13650–13662. Entrez PubMed 6815178
- Kaufman, B.T. e Gardiner, R.C. Studies on dihydrofolic reductase. I. Purification and properties of dihydrofolic reductase from chicken liver. J. Biol. Chem. 241 (1966) 1319–1328. Entrez PubMed 4379915
- Young, I.G. e Gibson, F. Regulation of the enzymes involved in the biosynthesis of 2,3-dihydroxybenzoic acid in Aerobacter aerogenes and Escherichia coli. Biochim. Biophys. Acta 177 (1969) 401–411. Entrez PubMed 4306838