Pentaclorofenolo
Il pentaclorofenolo (PCP) è un composto organoclorato usato come pesticida e disinfettante. Prodotto per la prima volta nel 1930, è stato commercializzato con diversi nomi commerciali. Si può trovare in due forme: PCP come tale oppure come sale sodico del PCP, che si dissolve facilmente in acqua.
| Pentaclorofenolo | |
|---|---|
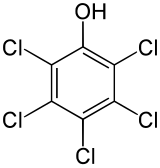 | |
| Nome IUPAC | |
| 2,3,4,5,6-Pentaclorofenolo | |
| Nomi alternativi | |
| Santophen, Pentachlorol, Chlorophen, Chlon, Dowicide 7, Pentacon, Penwar, Sinituho, Penta | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6HCl5O |
| Massa molecolare (u) | 266,34 g/mol |
| Aspetto | Solido bianco cristallino |
| Numero CAS | |
| Numero EINECS | 201-778-6 |
| PubChem | 992 |
| SMILES | Clc1c(O)c(Cl)c(Cl)c(Cl)c1Cl |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,978 g/cm3 a 22 °C |
| Solubilità in acqua | 0,020 g/L a 30 °C |
| Temperatura di fusione | 190–191 °C |
| Temperatura di ebollizione | 309–310 °C (dec.) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi R | 24/25-26-36/37/38-40-50/53 |
| Frasi S | 22-36/37-45-52-60-61[1] |
Chimica modifica
Il composto si presenta sotto forma di cristalli aghiformi bianchi. Questi cristalli, se scaldati, sviluppano un odore molto pungente e sublimano in aghetti. La molecola è praticamente insolubile in acqua, solubile in benzene e in etere di petrolio a freddo, molto solubile in etanolo e in etere.
La sostanza assorbe nell'ultravioletto (UV) alla lunghezza d'onda di 319 nm in soluzione acquosa alcalina, e di 295 nm in alcol. Lo spettro infrarosso (IR), registrato in bromuro di potassio (KBr), mostra assorbimenti identici a quelli di uno standard di riferimento (1307, 774, 1222, 711, 1196, 1553 cm1). Lo spettro di massa presenta frammenti principali a 266, 268, 264, 167, 165, 270, 202, 132 m/z. Con acido nitrico fumante si ottiene colorazione tra rosso e violetto.
Sintesi modifica
Il pentaclorofenolo può essere prodotto mediante clorurazione del fenolo in presenza di un catalizzatore (alluminio anidro o cloruro ferrico) ad una temperatura fino a circa 191 °C. Questo processo non si traduce in una completa clorazione e il PCP commercialmente disponibile è puro solo all'84-90%. I principali contaminanti sono altri fenoli policlorurati, dibenzo-p-diossine e policlorodibenzofurani. Alcune di queste sostanze sono ancora più tossiche del PCP stesso.
Usi modifica
Il composto viene impiegato, prevalentemente come sale sodico, come insetticida contro le termiti, defogliante prima della mietitura, diserbante, fungicida, molluschicida e antivegetativo in generale. È contenuto, come conservante, in prodotti come legno, prodotti del legno, tessuti, amido, destrine e colle.
Esposizione modifica
Esiste la possibilità di esporsi al pentaclorofenolo in ambiente lavorativo attraverso l'inalazione di aria contaminata oppure attraverso il contatto cutaneo con i prodotti di legno trattati con PCP. È possibile anche l'esposizione della popolazione generale, e ciò può avvenire attraverso il contatto con ambienti contaminati: ciò in particolare per coloro che vivoni in siti prossimi ad impianti di trattamento del legno e di rifiuti pericolosi. Altre importanti vie di esposizione sembrano essere l'inalazione di aria contaminata, l'ingestione di acqua di falda contaminata (usata come fonte di acqua potabile), l'ingestione di alimenti contaminati, e il contatto cutaneo con i terreni oppure i prodotti trattati con il composto chimico.
Tossicologia modifica
L'esposizione a breve termine a grandi quantità di PCP può causare effetti dannosi a carico del fegato, reni, sangue, polmoni, sistema nervoso centrale, sistema immunitario, tratto gastrointestinale. Studi sperimentali eseguiti hanno evidenziato una DL50 pari a 146 mg/kg peso corporeo nel ratto maschio e 175 mg/kg nel ratto femmina. Nell'uomo la dose letale minima è di circa 1 g. Concentrazioni plasmatiche superiori a 30 µg/ml sono considerate tossiche. In due casi letali, i rilevamenti post-mortem delle concentrazioni di pentaclorofenolo nei vari distretti sono stati i seguenti: 113 e 156 µg/ml nel sangue, 14 e 35 µg/g nel cervello, 123 µg/g nel rene, 94 e 134 µg/g nel fegato e 520 µg/ml nelle urine. In Gran Bretagna il valore massimo consentito di esposizione, in campo occupazionale, è pari a 0,5 mg/m3 per lunghi periodi e 1,5 mg/m3 per brevi periodi.
L'esposizione a pentaclorofenolo può comportare l'insorgenza di neoplasie maligne (linfoma non-Hodgkin,[2][3] mieloma multiplo, cancro del rene),[4][5][6][7] anemia aplastica,[8][9][10][11] pancreatiti,[12] emolisi intravascolare,[13] e orticaria. L'assorbimento involontario di pentaclorofenolo può portare ad avvelenamento acuto caratterizzato da innalzamento del metabolismo basale accompagnato da ipertermia, sudorazione profusa, sete, agitazione, nausea, dolore addominale, affaticamento, movimenti incoordinati, aumento della frequenza e della profondità della respirazione, tachicardia, coma. La morte sopraggiunge per insufficienza respiratoria.[14][15][16] Il contatto con PCP (in particolare sotto forma di vapore) può irritare la pelle, gli occhi e le alte vie respiratorie. L'esposizione a lungo termine a livelli bassi come quelli che si verificano sul posto di lavoro può invece causare danni al fegato, ai reni, al sangue e al sistema nervoso. Il trattamento dell'avvelenamento è di tipo sintomatico. Alcuni clinici ritengono che l'induzione di una diuresi forzata alcalina possa risultare vantaggiosa.
Il pentaclorofenolo viene prontamente assorbito per ingestione, inalazione o attraverso la cute, ed è eliminato attraverso le urine, in forma immodificata o come metabolita ossidato (tetracloroidrochinone) libero o coniugato. Solo circa il 4% di una dose assorbita viene eliminato attraverso le feci. Il pentaclorofenolo si distribuisce nell'organismo con un rapporto tra concentrazione plasmatica e concentrazione ematica di 1,8. Il legame con le proteine plasmatiche raggiunge il 99%. L'emivita plasmatica è di 30 ore.
Determinazione nei liquidi biologici modifica
Il pentaclorofenolo può essere quantificato nel plasma o nelle urine. L'esame viene normalmente eseguito mediante cromatografia liquida ad alta risoluzione,[17][18] o tramite gascromatografia con cattura elettronica[19] o rilevazione spettrometrica di massa. In situazioni di esposizione croniche l'urina contiene prevalentemente pentaclorofenolo coniugato, è pertanto consigliato prima di tutto eseguire l'idrolisi dei campioni.[19]
Note modifica
- ^ Pentachlorophenol 97% | Sigma-Aldrich
- ^ MH. Greene, LA. Brinton; JF. Fraumeni; R. D'Amico, Familial and sporadic Hodgkin's disease associated with occupational wood exposure., in Lancet, vol. 2, n. 8090, Set 1978, pp. 626-7, PMID 80546.
- ^ L. Hardell, Relation of soft-tissue sarcoma, malignant lymphoma and colon cancer to phenoxy acids, chlorophenols and other agents., in Scand J Work Environ Health, vol. 7, n. 2, Giu 1981, pp. 119-30, PMID 7313616.
- ^ GS. Cooper, S. Jones, Pentachlorophenol and cancer risk: focusing the lens on specific chlorophenols and contaminants., in Environ Health Perspect, vol. 116, n. 8, Ago 2008, pp. 1001-8, DOI:10.1289/ehp.11081, PMID 18709150.
- ^ E. Lynge, Cancer in phenoxy herbicide manufacturing workers in Denmark, 1947-87--an update., in Cancer Causes Control, vol. 4, n. 3, Mag 1993, pp. 261-72, PMID 8318642.
- ^ M. Kogevinas, H. Becher; T. Benn; PA. Bertazzi; P. Boffetta; HB. Bueno-de-Mesquita; D. Coggon; D. Colin; D. Flesch-Janys; M. Fingerhut; L. Green, Cancer mortality in workers exposed to phenoxy herbicides, chlorophenols, and dioxins. An expanded and updated international cohort study., in Am J Epidemiol, vol. 145, n. 12, Giu 1997, pp. 1061-75, PMID 9199536.
- ^ PA. Demers, HW. Davies; MC. Friesen; C. Hertzman; A. Ostry; R. Hershler; K. Teschke, Cancer and occupational exposure to pentachlorophenol and tetrachlorophenol (Canada)., in Cancer Causes Control, vol. 17, n. 6, Ago 2006, pp. 749-58, DOI:10.1007/s10552-006-0007-9, PMID 16783603.
- ^ HJ. Roberts, Pentachlorophenol-associated aplastic anemia, red cell aplasia, leukemia and other blood disorders., in J Fla Med Assoc, vol. 77, n. 2, Feb 1990, pp. 86-90, PMID 2106570.
- ^ HJ. Roberts, Aplastic anemia due to pentachlorophenol and tetrachlorophenol., in South Med J, vol. 56, Giu 1963, pp. 632-5, PMID 13974304.
- ^ HJ. Roberts, Aplastic anemia due to pentachlorophenol., in N Engl J Med, vol. 305, n. 27, Dic 1981, pp. 1650-1, PMID 7312014.
- ^ HJ. Roberts, Aplastic anemia and red cell aplasia due to pentachlorophenol., in South Med J, vol. 76, n. 1, Gen 1983, pp. 45-8, PMID 6823577.
- ^ RG. Cooper, MB. Macauley, Pentachlorophenol pancreatitis., in Lancet, vol. 1, n. 8270, Feb 1982, p. 517, PMID 6121177.
- ^ AB. Hassan, H. Seligmann; HM. Bassan, Intravascular haemolysis induced by pentachlorophenol., in Br Med J (Clin Res Ed), vol. 291, n. 6487, Lug 1985, pp. 21-2, PMID 3926044.
- ^ AT. Proudfoot, Pentachlorophenol poisoning., in Toxicol Rev, vol. 22, n. 1, 2003, pp. 3-11, PMID 14579543.
- ^ C. Carballo Fernández, E. Murias Taboada; D. Vila Fernández; MJ. Guillén Vázquez; F. Peña Marcos; L. Amador Barciela, [Pentachlorophenol poisoning. Report of 4 cases and review of the literature]., in An Med Interna, vol. 17, n. 5, Mag 2000, pp. 257-60, PMID 10859827.
- ^ PG. Jorens, PJ. Schepens, Human pentachlorophenol poisoning., in Hum Exp Toxicol, vol. 12, n. 6, Nov 1993, pp. 479-95, PMID 7904464.
- ^ DA. Kalman, Determination of pentachlorophenol and 2,3,4,6-tetrachlorophenol in human urine by high resolution gas chromatography., in J Chromatogr Sci, vol. 22, n. 10, Ott 1984, pp. 452-5, PMID 6501528.
- ^ DL. Rick, CF. Licht; LP. McCarty, Determination of phenol and pentachlorophenol in plasma and urine samples by gas liquid chromatography., in J Anal Toxicol, vol. 6, n. 6, pp. 297-300, PMID 7162140.
- ^ a b SL. Wagner, LR. Durand; RD. Inman; U. Kiigemagi; ML. Deinzer, Residues of pentachlorophenol and other chlorinated contaminants in human tissues: analysis by electron capture gas chromatography and electron capture negative ion mass spectrometry., in Arch Environ Contam Toxicol, vol. 21, n. 4, Nov 1991, pp. 596-606, PMID 1759853.
Altri progetti modifica
- Wikimedia Commons contiene immagini o altri file su pentaclorofenolo
Collegamenti esterni modifica
- (EN) pentachlorophenol, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh85099614 · GND (DE) 4123922-2 · J9U (EN, HE) 987007533823505171 · NDL (EN, JA) 00575320 |
|---|