Sindrome di Wolff-Parkinson-White
La sindrome di Wolff Parkinson White (WPW) è una malattia congenita da anomala conduzione cardiaca; è caratterizzata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine a episodi di tachicardia sporadica. La prevalenza media è stimata in 1/450 e quindi la sindrome non è considerata una malattia rara.
| Sindrome di Wolff-Parkinson-White | |
|---|---|
 | |
| Specialità | cardiologia |
| Classificazione e risorse esterne (EN) | |
| OMIM | 194200 |
| MeSH | D014927 |
| MedlinePlus | 000151 |
| eMedicine | 159222 |
| Eponimi | |
| Louis Wolff John Parkinson Paul Dudley White | |
La sindrome di WPW colpisce soprattutto maschi (70% dei casi) in giovane età. Durante la vita fetale, gli atri vengono collegati ai ventricoli da numerosi fasci che scompaiono dopo la nascita, fatta eccezione per uno, il fascio di His. Tuttavia, in alcuni pazienti possono persistere anche altri fasci. Queste vie accessorie aggirano il nodo atrio-ventricolare e causano una pre-eccitazione ventricolare e, in alcuni casi, episodi di tachicardia, che possono interrompersi spontaneamente oppure necessitano di un trattamento farmacologico.
La sindrome di WPW può essere sporadica o familiare. La forma familiare è difficilmente identificabile, in quanto le vie accessorie non sono sempre attive. Mutazioni del gene PRKAG2 sono state associate a forme familiari della sindrome di WPW. La diagnosi viene spesso posta in base al riscontro dei disturbi del ritmo. Oltre a essi, l'ECG può mostrare tre segni: la mancanza della via lenta atrio-ventricolare (intervallo PR corto, < 0,12 secondi), una pre-eccitazione ventricolare (onda delta all'inizio del complesso QRS), una stimolazione anormale dei ventricoli (complesso QRS più largo> 0,12 secondi tra l'inizio dell'onda delta e la fine di QRS). Queste anomalie dell'ECG corrispondono a un fascio anomalo direttamente collegato agli atri e ai ventricoli. Se il fascio collega l'atrio al fascio di His, l'ECG rileva un intervallo PR corto (< 0,12 secondi), con un complesso QRS normale. Si tratta di una variante della sindrome di WPW, che prende il nome di sindrome di Lown-Ganong-Levine.
Fisiopatologia modifica
Negli individui normali l'attività elettrica cardiaca si avvia nel nodo seno-atriale, localizzato nell'atrio destro, si propaga attraverso il nodo atrio-ventricolare e attraverso il fascio di His ai ventricoli. Il nodo atrio-ventricolare funziona come un cancello, limitando l'attività elettrica che giunge ai ventricoli. Questa funzione è molto importante, poiché se il segnale in partenza dall'atrio aumenta di frequenza (come durante la fibrillazione atriale o il flutter atriale), il nodo limita la frequenza ventricolare. Per esempio, se gli atri si attivano 300 volte al minuto, metà degli impulsi elettrici saranno bloccati dal nodo, cosicché i ventricoli pulseranno solo 150 volte al minuto.
La caratteristica elettrofisiologica alla base di quest'importante proprietà del nodo atrio-ventricolare è una minore velocità di conduzione dei singoli impulsi, e questo si esprime con il tratto PR nell'elettrocardiogramma, che è il tempo che intercorre tra l'attivazione atriale e quella ventricolare.
I soggetti con la sindrome di WPW hanno un percorso accessorio che collega atri e ventricoli, oltre al nodo atrio-ventricolare. Questo percorso accessorio è noto come fascio di Kent. Questo fascio accessorio non mostra le stesse proprietà di rallentamento del nodo atrio-ventricolare, e può condurre gli impulsi elettrici molto più rapidamente di quest'ultimo. Riprendendo l'esempio di prima, se un soggetto ha una frequenza atriale di 300 battiti al minuto, il fascio accessorio può condurre tutti gli impulsi fino ai ventricoli, che così si attivano 300 volte al minuto. Questo evento è di per sé sfavorevole: le frequenze cardiache, infatti, tanto più sono elevate tanto più possono alterare l'efficienza emodinamica. In alcuni casi, la concomitanza del fascio accessorio con aritmie cardiache di varia origine può portare a fenomeni di rientro atrioventicolare e all'instaurarsi di fibrillazione ventricolare, causa di morte cardiaca improvvisa.
Diagnosi modifica
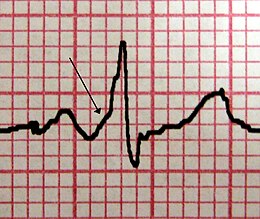
La sindrome di WPW è frequentemente diagnosticata tramite un elettrocardiogramma (ECG) in un individuo asintomatico. In questi casi si manifesta come un'onda delta, che è l'ampliamento della fase di ascesa del QRS associato all'accorciamento dell'intervallo PR. Tutto questo è dovuto al fluire dell'impulso elettrico attraverso la via accessoria piuttosto che attraverso il nodo atrio-ventricolare.
Se il paziente accusa episodi di fibrillazione atriale, l'ECG mostra una tachicardia rapida polimorfica (senza torsione di punta). Questa combinazione di fibrillazione atriale e sindrome di WPW è considerata pericolosa, e molti farmaci antiaritmici sono controindicati.
Quando un soggetto è in normale ritmo sinusale le caratteristiche della sindrome di WPW sono un intervallo PR corto, uno slargamento del complesso QRS (più di 110 ms in lunghezza) con ampliamento della fase di ascesa del QRS stesso, e cambiamenti della ripolarizzazione che si riflettono in alterazioni del tratto ST e dell'onda T.
In soggetti affetti l'attività elettrica che incomincia nel nodo seno-atriale passa attraverso il fascio accessorio tanto bene quanto nel nodo atrio-ventricolare. Poiché il fascio accessorio non blocca l'impulso quanto il nodo, i ventricoli vengono attivati da questo, e subito dopo dal nodo. Questo causa le alterazioni ECG sopra descritte.
I pazienti con sindrome di WPW spesso hanno più di una via accessoria, e in alcuni possono essere anche più di otto; questo è stato dimostrato in soggetti affetti dall'anomalia di Ebstein.
La sindrome di WPW è talora associata alla neuropatia ottica ereditaria di Leber (LHON), una forma di malattia mitocondriale.[1]
Stratificazione del rischio modifica
La terapia è basata sulla stratificazione del rischio individuale. La stratificazione del rischio serve a valutare quali individui con la sindrome di WPW sono a rischio di morte cardiaca improvvisa, che in questi soggetti è dovuta alla propagazione ad alto ritmo di una aritmia atriale ai ventricoli.
Una buona anamnesi deve essere raccolta per determinare l'eventuale presenza di fattori individuali suggestivi di precedenti episodi di sincope inspiegabile, perdita di coscienza e/o palpitazioni (percepite come battiti cardiaci irregolari). Questi eventi possono essere dovuti a tachicardia dovuta alla via accessoria.
Soggetti con la sindrome di WPW nei quali l'onda delta sparisce con un incremento della frequenza cardiaca sono considerati a basso rischio di morte cardiaca improvvisa; questo perché la perdita dell'onda delta mostra che la via accessoria non può condurre ad alta frequenza (in direzione anterograda). Questi soggetti non hanno una elevata velocità di conduzione attraverso la via accessoria durante gli episodi di fibrillazione atriale.
La stratificazione del rischio è meglio precisata tramite uno studio elettrofisiologico endocavitario in un ambulatorio di elettrofisiologia cardiaca. Si tratta di una procedura invasiva, durante la quale la velocità di conduzione dell'impulso attraverso la via accessoria è determinata stimolando gli atri e inducendo una fibrillazione atriale temporanea.
I fenomeni legati a un alto rischio che possono dimostrarsi durante questo esame includono un periodo refrattario della via accessoria inferiore a 270 ms, vie accessorie multiple, vie accessorie locate vicino al setto, e una suscettibilità alla tachicardia sopraventricolare. I soggetti con uno qualsiasi di questi fattori sono considerati ad alto rischio di morte cardiaca improvvisa e dovrebbero essere trattati in modo consono.[2]
Non è chiaro se la stratificazione del rischio invasiva tramite stimolazione elettrica programmata sia necessaria nei soggetti asintomatici.[3]
Mentre alcuni richiedono questo esame per tutti i soggetti al di sotto dei 35 anni, altri lo propongono solo a quanti hanno una storia suggestiva per tachiaritmia, visto che l'incidenza di morte cardiaca improvvisa è bassa.
Terapia modifica
In acuto i soggetti con sindrome di WPW che abbiano una tachiaritmia possono necessitare di una cardioversione se le loro condizioni sono critiche, o, se più stabili, di sola terapia medica. I pazienti con fibrillazione atriale e rapida risposta ventricolare sono spesso trattati con amiodarone o procainamide per stabilizzare la frequenza. L'adenosina e altri bloccanti del nodo atrio-ventricolare possono essere inutili nella fibrillazione atriale in un soggetto con sindrome di WPW: questi includono adenosina, diltiazem, verapamil e altri calcio-antagonisti e beta-bloccanti. Pazienti tachicardici con complesso QRS stretto possono essere cardiovertiti, oppure si può effettuare un tentativo con l'adenosina a patto che l'equipaggiamento da cardioversione sia immediatamente disponibile.
Il trattamento definitivo della sindrome di WPW è la distruzione della via accessoria con un'ablazione transcatetere con radiofrequenza. Questa procedura è svolta da cardiologi specializzati in elettrofisiologia; non può essere fatta a tutti i soggetti affetti per i rischi legati alla procedura stessa.
L'adenosina è controindicata nei pazienti in fibrillazione atriale o flutter atriale con storia di sindrome di WPW.
Se fatta da mani esperte, l'ablazione tramite radiofrequenza ha un alto indice di successo.[4]
Se l'ablazione ha successo, il paziente è considerato guarito. Si hanno ricadute in meno del 5% dei soggetti dopo ablazione completa.[4]
I soggetti con una sottostante anomalia di Ebstein possono sviluppare altre vie accessorie durante il decorso della patologia di base.
Note modifica
- ^ Mashima Y, Kigasawa K, Hasegawa H, Tani M, Oguchi Y., High incidence of pre-excitation syndrome in Japanese families with Leber's hereditary optic neuropathy, in Clinical Genetics, vol. 50, n. 6, 1996, pp. 535-7, PMID 9147893.
- ^ Pappone C, Santinelli V, Manguso F, Augello G, Santinelli O, Vicedomini G, Gulletta S, Mazzone P, Tortoriello V, Pappone A, Dicandia C, Rosanio S., A randomized study of prophylactic catheter ablation in asymptomatic patients with the Wolff-Parkinson-White syndrome, in New England Journal of Medicine, vol. 349, n. 19, 2003, pp. 1803-11, PMID 14602878.
- ^ Campbell RM, Strieper MJ, Frias PA, Collins KK, Van Hare GF, Dubin AM, Survey of current practice of pediatric electrophysiologists for asymptomatic Wolff-Parkinson-White syndrome, in Pediatrics, vol. 111, n. 3, 2003, pp. e245-7, PMID 12612279.
- ^ a b Pappone C, Lamberti F, Santomauro M, Stabile G, De Simone A, Turco P, Pannain S, Loricchio ML, Rotunno R, Chiariello M, Ablation of paroxysmal tachycardia in Wolff-Parkinson-White syndrome, in Cardiologia, vol. 38, 12 Suppl 1, 1993, pp. 189-97, PMID 8020017.
Bibliografia modifica
- Joseph C. Segen, Dizionario di medicina moderna, Milano, McGraw-Hill, 2006, ISBN 978-88-386-3917-3.
- Douglas M. Anderson, A. Elliot Michelle, Mosby's medical, nursing, & Allied Health Dictionary sesta edizione, New York, Piccin, 2004, ISBN 88-299-1716-8.
- Harrison, Principi di Medicina Interna (il manuale - 16ª edizione), New York - Milano, McGraw-Hill, 2006, ISBN 88-386-2459-3.
- Hurst, Il Cuore (il manuale - 11ª edizione), Milano, McGraw-Hill, 2006, ISBN 978-88-386-2388-2.
- Eugene Braunwald, Malattie del cuore (7ª edizione), Milano, Elsevier Masson, 2007, ISBN 978-88-214-2987-3.
- Aldo Zangara, Terapia medica ragionata delle malattie del cuore e dei vasi, Padova, Piccin, 2000, ISBN 88-299-1501-7.
- Daniele Bracchetti, Guadagna RF, Calmieri M, Le aritmie cardiache clinica, terapia medica e invasiva terza edizione, Padova, Piccin, 1999, ISBN 88-299-1378-2.
- Marcello Costantini, L'elettrocardiogramma dalle basi fisiologiche alla facile interpretazione seconda edizione, Milano, McGraw-Hill, 2006, ISBN 978-88-386-1669-3.
- Fiorenzo Gaita e Giuseppe Oreto, La sindrome di Wolff-Parkinson-White, Torino, Centro scientifico, 2000, ISBN 88-7640-461-9.
- Mario Cariello, La sindrome di Wolff, Parkinson, White ed i suoi riflessi medico-sociali e legali, in Folia medica, vol. 46, n. 6, Napoli, V. Idelson, 1963, pp. 492-503.
Voci correlate modifica
Altri progetti modifica
- Wikimedia Commons contiene immagini o altri file su sindrome di Wolff-Parkinson-White
| Controllo di autorità | Thesaurus BNCF 24315 · LCCN (EN) sh85147229 · BNF (FR) cb12173227c (data) · J9U (EN, HE) 987007558557405171 · NDL (EN, JA) 00576080 |
|---|