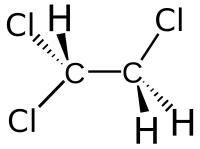
1,1,2-tricloroetano
L'1,1,2-tricloroetano, o tricloruro di vinile, è un solvente organocloruro con formula molecolare C2H3Cl3. Appartiene alla classe dei composti organici detti alogenuri alchilici. Uno dei 9 cloroetani, cioè derivati dell'etano in cui tre dei sei idrogeni sono sostituiti da cloro.
| 1,1,2-tricloroetano | |
|---|---|
 | |
| Nome IUPAC | |
| 1,1,2-tricloroetano[1][2][3] | |
| Abbreviazioni | |
| 1,1,2-TCA | |
| Nomi alternativi | |
| tricloruro di vinile, beta-tricloroetano | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H3Cl3 |
| Massa molecolare (u) | 133.40[4] |
| Aspetto | liquido incolore, odore dolce, simile al cloroformio |
| Numero CAS | Immagine_3d Immagine_3d |
| Numero EINECS | 201-166-9 |
| PubChem | 6574 |
| SMILES | ClCC(Cl)Cl |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1.435 |
| Solubilità in acqua | 0.4% (20 °C)[5] |
| Temperatura di fusione | -37 °C |
| Temperatura di ebollizione | 110-115 °C |
| Tensione di vapore (Pa) a 295 K | 19 mmHg (20 °C)[5] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 302+312 - 331 - 351 - 412 - EUH066 |
| Consigli P | 201 - 273 - 280 - 302+352+312 - 304+340+311 - 308+313 |
È un liquido trasparente, profumato che non dissolve in acqua, ma è solubile in molti solventi organici.
È usato come solvente e come intermedio nella sintesi dell'1,1-dicloroetano.
1,1,2-TCA è un depressivo per il sistema nervoso centrale e l'inalazione dei vapori può causare vertigini, sonnolenza, mal di testa, nausea, mancanza di respiro, incoscienza, o tumore.[6]
Sintesi modifica
L'1,1,2-tricloroetano può essere prodotto da clorurazione dell'1,2-dicloroetano.
- CH2ClCH2Cl + Cl2 → CHCl2CH2Cl + HCl
Tossicologia modifica
Il tricloroetano può essere nocivo per inalazione, ingestione e contatto con la pelle. È un irritante per le vie respiratorie e per gli occhi. Sebbene attualmente non esistano studi definitivi, il tricloroetano dovrebbe essere trattato come un potenziale carcinogeno in quanto prove di laboratorio suggeriscono che gli idrocarburi clorurati a basso peso molecolare possono essere cancerogenici.[6]
L'OSHA e la NIOSH hanno imposto un limite nell'ambiente di lavoro di esposizione al tricloroetano pari a 10 ppm su una media ponderata nel tempo di otto ore.[5] Oltre questi limiti viene considerato il rischio potenziale di essere cancerogeno.
Cloroetani modifica
Riportiamo i 6 cloroetani e i 3 isomeri di struttura
- Cloroetano
- 1,1-dicloroetano
- 1,2-dicloroetano (isomero)
- 1,1,1-tricloroetano
- 1,1,2-tricloroetano (isomero)
- 1,1,1,2-tetracloroetano
- 1,1,2,2-tetracloroetano (isomero)
- Pentacloroetano
- Esacloroetano
Note modifica
- ^ (EN) Favre Henri A. e Powell Warren H. (a cura di), Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013, IUPAC Chemical Nomenclature and Structure Representation Division, Londra, IUPAC/RSC, 2013, ISBN 978-0-85404-182-4.
- ^ (EN) PubChem Compound, 1,1,2-Trichloroethane - Compound Summary, su pubchem.ncbi.nlm.nih.gov, National Center for Biotechnology Information, 27 Marzo 2005. URL consultato il 9 Maggio 2021.
- ^ (EN) Chemical Entities of Biological Interest, CHEBI:36018 - 1,1,2-trichloroethane, su ebi.ac.uk, EBI (UK), 28-07-2014. URL consultato il 09-05-2021.
- ^ (EN) IUPAC Commission on Isotopic Abundances and Atomic Weights., Atomic weights of the elements 2017, su Queen Mary University of London.
- ^ a b c (EN) NIOSH Pocket Guide to Chemical Hazards, 1,1,2-Trichloroethane, su cdc.gov, NIOSH.
- ^ a b (EN) Safety (MSDS) data for 1,1,2-trichloroethane (PDF), su spectrumchemical.com, TCI AMERICA. URL consultato il 09-05-2021.
Voci correlate modifica
Altri progetti modifica
- Wikimedia Commons contiene immagini o altri file su 1,1,2-tricloroetano
Collegamenti esterni modifica
- (EN) 1,1,2-trichloroethane, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.

