Acido vaccenico
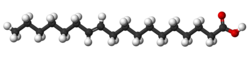
L'acido vaccenico (o acido 11-ottadecenoico) è un acido grasso a 18 atomi di carbonio, avente formula bruta C18H34O2. Individuato da S.H.Bertram nel 1928 è stato la prima dimostrazione della presenza di isomeri trans nei grassi dei ruminanti, in particolare nel latte della vacca, da cui deriva il nome[1].
| Acido vaccenico | |
|---|---|
 | |
| Nome IUPAC | |
| acido 11E-ottadecenoico | |
| Nomi alternativi | |
| acido vaccenico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C18H34O2 |
| Numero CAS | |
| Numero EINECS | 211-758-9 |
| PubChem | 5281127 |
| SMILES | CCCCCCC=CCCCCCCCCCC(=O)O |
| Indicazioni di sicurezza | |
Chimica modifica
Si forma come intermedio durante la bioidrogenazione dell'acido linoleico ad acido stearico ad opera del Butyrivibrio fibrisolvens ed altri batteri del rumine. Dall'acido vaccenico si ottiene l'acido rumenico, acido linoleico coniugato cis9 trans11, tramite azione enzimatica.[1]
Si presenta anche nella forma cis, nota anche con il nome: acido asclepico con temperatura di fusione di circa 15 °C[2]. In particolare lo stereoisomero cis è presente nel cervello del cavallo dove svolgerebbe azione emolitica[3] ed in alcuni oli vegetali come quello di macadamia o di olivello spinoso, che possono contenerne anche più del 2%.[4] L'isomero trans, con temperatura di fusione di circa 44 °C, non è normalmente presente negli oli vegetali.
Uno studio dell’Università di Chicago del 2023 ha scoperto che l’acido trans-vaccenico migliora l’immunità antitumorale attivando le cellule T CD8+. Questo effetto si ottiene disattivando un recettore GPR43, che attiva invece la via CREB.[5][6]
Funzioni biologiche modifica
Meccanicamente, il TVA inattiva il recettore della superficie cellulare GPR43, un recettore immunomodulatore accoppiato a proteine G attivato dai suoi ligandi di acidi grassi a catena corta. Il TVA antagonizza quindi gli agonisti degli acidi grassi a catena corta di GPR43, portando all'attivazione dell'asse cAMP-PKA-CREB per una migliore funzione delle cellule T CD8+.
Questi risultati rivelano che il TVA derivato dalla dieta rappresenta un meccanismo per la riprogrammazione estrinseca dell’ospite delle cellule T CD8+ in contrapposizione agli acidi grassi a catena corta derivati dal microbiota intestinale intraospite. La TVA ha quindi un potenziale traslazionale per il trattamento dei tumori.[5][6]
Dosaggio modifica
Il rilevamento e la determinazione del contenuto dell'acido vaccenoico sono generalmente effettuati con la gascromatografia dell'estere metilico; inoltre, si ottiene una separazione degli isomeri insaturi con cromatografia a strato sottile su nitrato d'argento.[7]
Note modifica
- ^ a b F. Destaillats, E. Buyukpamukcu, P.-A. Golay, F. Dionisi, F. Giuffrida, Letter to the Editor: Vaccenic and Rumenic Acids, A Distinct Feature of Ruminant Fats, in Journal of Dairy Science, vol. 88, n. 449, 2005, p. 449, DOI:10.3168/jds.S0022-0302(05)72705-3.
- ^ Common (non-systematic) Names for Fatty Acids (PDF), su aocs.files.cms-plus.com. URL consultato il 14 novembre 2015 (archiviato dall'url originale il 17 novembre 2015).
- ^ "vaccènico", Sapere.it
- ^ A.Johansson, P.Laakso, H.Kallio, Zeitschrift fuer Lebensmittel-Untersuchung; Foschg. A., vol. 204, p. 300-307.
- ^ a b Hao Fan, Siyuan Xia, Junhong Xiang, Yuancheng Li, Matthew O. Ross, Seon Ah Lim, Fan Yang, Jiayi Tu, Lishi Xie, Urszula Dougherty, Freya Q. Zhang, Zhong Zheng, Rukang Zhang, Rong Wu, Lei Dong, Rui Su, Xiufen Chen, Thomas Althaus, Peter A. Riedell, Patrick B. Jonker, Alexander Muir, Gregory B. Lesinski, Sarwish Rafiq, Madhav V. Dhodapkar, Wendy Stock, Olatoyosi Odenike, Anand A. Patel, Joseph Opferman, Takemasa Tsuji, Junko Matsuzaki, Hardik Shah, Brandon Faubert, Shannon E. Elf, Brian Layden, B. Marc Bissonnette, Yu-Ying He, Justin Kline, Hui Mao, Kunle Odunsi, Xue Gao, Hongbo Chi, Chuan He e Jing Chen, Trans-vaccenic acid reprograms CD8+ T cells and anti-tumour immunity, in Nature, vol. 623, n. 7989, 2023, pp. 1034–1043, DOI:10.1038/s41586-023-06749-3, ISSN 1476-4687, PMC 10686835, PMID 37993715.
- ^ a b Trans-vaccenic Acid Reprograms CD8+ T Cells and Enhances Antitumor Immunity, in Cancer Discovery, 8 dicembre 2023, p. OF1, DOI:10.1158/2159-8290.CD-RW2023-192, ISSN 2159-8290, PMID 38064352.
- ^ B. Breuer, T. Stuhlfauth e H. P. Fock, Separation of fatty acids or methyl esters including positional and geometric isomers by alumina argentation thin-layer chromatography, in Journal of Chromatographic Science, vol. 25, n. 7, 1987, pp. 302–306, DOI:10.1093/chromsci/25.7.302, ISSN 0021-9665, PMID 3611285.
Altri progetti modifica
- Wikimedia Commons contiene immagini o altri file su acido vaccenico
Collegamenti esterni modifica
- LBF18107SC02, su lipidbank_wiki, 29 settembre 2010. URL consultato il 24 gennaio 2024.
- trans-Vaccenic acid =99 capillaryGC 693-72-1, su www-sigmaaldrich-com.translate.goog. URL consultato il 24 gennaio 2024.
- cis-Vaccenic acid = 97 capillary GC, oil 506-17-2, su www-sigmaaldrich-com.translate.goog. URL consultato il 24 gennaio 2024.
- PlantFAdb: 18:1-delta-11c; Asclepic acid; cis-Vaccenic acid; 11-Octadecenoic acid, (11Z)-; 11-Octadecenoic acid, (Z)-; 11-Octadecenoic acid, cis-; (Z)-11-Octadecenoic acid; (Z)-Octadec-11-enoic acid; 11-cis-Octadecenoic acid; 11-cis-Vaccenic acid; Asclepic acid; C18:1; cis-11-Octadecenoic acid; cis-11-Vaccenic acid; cis-Vaccenic acid; cis-Vaccenic acid; cis--delta-11-Octadecenoic acid; -delta-11-cis-Octadecenoic acid, su plantfadb-org.translate.goog. URL consultato il 24 gennaio 2024.