Trabectedina
La trabectedina (nota anche come ecteinascidin 743 o ET-743) è un farmaco antitumorale, chimicamente una tetraidro isochinolina, scoperto nel 1969 e ricavato da un'ascidia marina caraibica: la Ecteinascidia turbinata.[1]
| Trabectedina | |
|---|---|
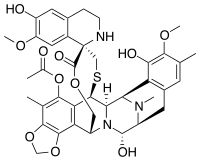 | |
| Nome IUPAC | |
| R,6R,6aR,7R,13S,14S,16R)-6',8,14-trihydroxy-7',9-dimethoxy-4,10,23-trimethyl-19-oxo-3',4',6,7,12,13,14,16-octahydrospiro[6,16-(epithiopropano-oxymethano)-7,13-imino-6aH-1,3-dioxolo[7,8]isoquino[3,2-b][3]benzazocine-20,1'(2H)-isoquinolin]-5-yl acetate | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C39 H43N3O11S |
| Massa molecolare (u) | 761.84 g·mol-1 |
| Numero CAS | |
| Numero EINECS | 695-026-8 |
| Codice ATC | LO1 |
| PubChem | 108150 e 89263850 |
| DrugBank | DBDB05109 |
| SMILES | CC1=C(C(=C2C3C4C5C6=C(C(N4C(C(N3C)CC2=C1)O)COC(=O)C7(CS5)C8=CC(=C(C=C8CCN7)O)OC)C9=C(C(=C6OC(=O)C)C)OCO9)O)OC e O=C(OC=1C(=C2OCOC2=C3C1C4SCC5(NCCC6=CC(O)=C(OC)C=C65)C(=O)OCC3N7C(O)C8N(C)C(C9=C(O)C(OC)=C(C=C9C8)C)C74)C)C |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | °C |
| Temperatura di ebollizione | °C |
| Dati farmacologici | |
| Categoria farmacoterapeutica | Antitumorale |
| Modalità di somministrazione | I.V. |
| Dati farmacocinetici | |
| Metabolismo | epatico |
| Emivita | 180 ore |
| Indicazioni di sicurezza | |
È venduto dalle aziende Zeltia e Johnson & Johnson con il nome commerciale di Yondelis.
Farmacodinamica
modificaCome molti altri chemioterapici interagenti con il DNA, la trabectedina produce delle profonde perturbazioni del ciclo cellulare, che inducono la cellula alla morte cellulare programmata (apoptosi)[1].
In particolare, il composto induce rallentamento della progressione del ciclo cellulare dalla fase G1 alla fase G2, un'inibizione della sintesi del DNA e un blocco marcato in fase premitotica (G2), che non sembra p53 dipendente. È stato inoltre dimostrato che le cellule in fase G1 sono ipersensibili al farmaco rispetto a quelle che si trovano in fase S e G2-M[2].
Il meccanismo attraverso il quale la trabectedina esplica attività antitumorale è tuttavia molto complesso e si articola in quattro modalità:
- legame al solco minore del DNA
- interferenza con i meccanismi di riparazione del DNA
- modulazione della trascrizione
- effetti sul microambiente tumorale
Legame con il DNA
modificaIl composto è di fatto il primo di una nuova classe di agenti leganti il DNA: pur agendo in modo simile agli alchilanti, differisce da questi, che legano il solco maggiore del DNA e formano crosslinks con la guanina in posizione N7 o O6, poiché si lega al solco minore del DNA, in particolare alla guanina in posizione N2. Il legame del farmaco al solco minore determina la formazione di addotti e induce un ripiegamento del DNA verso il solco maggiore con una modalità che sembra esclusiva di questo composto[3].
Interferenza con i sistemi di riparazione del DNA
modificaL'anello C del farmaco non si lega al DNA e sembra invece interagire con differenti proteine leganti il DNA, tra le quali membri del sistema NER (Nucleotide Excision Repair)[4]. Il sistema NER riconosce normalmente il DNA danneggiato e determina il reclutamento di diversi fattori che si portano a livello del sito danneggiato al fine di riparare le distorsioni presenti nella doppia elica. Tale sistema interviene frequentemente nei danni indotti da radiazioni ultraviolette, da alchilanti e altri cancerogeni, riparando efficacemente il danno. Nel caso degli addotti prodotti dalla trabectedina, al contrario, il NER non opta per la riparazione, ma piuttosto per l'induzione della morte cellulare, favorendo così l'azione del farmaco[5]. Pertanto, diversamente dagli altri agenti interagenti col DNA, i quali richiedono un sistema NER poco efficiente, la trabectedina richiede un sistema NER efficiente per poter esercitare appieno la sua azione[2].
E' importante sottolineare che, comunemente ad altri composti a meccanismo d'azione simile (come gli alchilanti), la riparazione tramite ricombinazione omologa (HR- Homologue Recombination) e tramite ricombinazione non-omologa (NHR - Non Homologue Recombination) gioca un ruolo importante e cellule deficienti di tale sistema di riparazione risultano più sensibili all'azione della trabectedina[6]. Deficienze a carico del sistema di mismatch repair non influiscono invece sull'attività citotossica del farmaco[7].
Modulazione della trascrizione
modificaIl farmaco agisce anche a livello della trascrizione. Modificazioni nella struttura del DNA indotti dalla trabectedina sembrerebbero infatti impedire il riconoscimento di fattori di trascrizione a specifiche sequenze consenso ricche in guanina e citosina[8]. A livello cellulare la trabectedina non sembra comunque interferire con la trascrizione costituzionale, ma solo con quella di geni attivati. Ulteriori studi hanno inoltre evidenziato che, sebbene il farmaco leghi il solco minore del DNA, esplica effetti anche su promotori regolati da fattori di trascrizione che legano il solco maggiore del DNA. La trabectedina, inoltre, è selettivamente attiva solo su alcuni geni attivati e su questi favorisce o inibisce a sua volta i processi di trascrizione[9]. Il fatto che il composto induca up-regolazione o down-regolazione sugli stessi geni di linee cellulari differenti suggerisce comunque la presenza di cofattori cellula-specifici, che giocano un ruolo importante nel modulare la capacità del farmaco di agire sulla trascrizione[1].
Effetti sul microambiente tumorale
modificaA basse concentrazioni il farmaco risulta agire anche sul micro-ambiente tumorale: appare infatti ridurre la produzione di fattori pro-infiammatori (CCL2) e interleuchine (IL6) da parte di monociti e macrofagi[10]. CCL2 gioca un ruolo importante nel reclutamento di monociti sul sito tumorale, mentre IL6 è un fattore di crescita per molti tumori. Questi dati sono stati recentemente confermati da studi su linee cellulari di liposarcoma[11].
Impiego clinico
modificaIl 17 settembre 2007 l'Agenzia europea per i medicinali (EMA)[12] ha rilasciato autorizzazione all'immissione in commercio per Yondelis, nel trattamento di:
- sarcomi dei tessuti molli (principalmente liposarcoma e leiomiosarcoma)[13]
- carcinoma dell'ovaio.[14]
Per quanto riguarda il sarcoma dei tessuti molli avanzato, si prevede l'impiego del farmaco dopo fallimento terapeutico di antracicline e ifosfamide o per pazienti non candidabili a tale trattamento. Per quanto riguarda invece il carcinoma ovarico, la trabectedina viene impiegata in associazione con doxorubicina liposomiale pegilata (PLD) nel trattamento di pazienti con recidiva di cancro ovarico, sensibili al platino. Anche la Food and Drug Administration americana ha concesso lo status di farmaco orfano alla trabectedina per il trattamento di queste due patologie. Mentre in Russia e Corea del Sud[15][16] il composto è approvato per il trattamento del sarcoma avanzato. Sono inoltre in corso, o conclusi da poco, studi clinici per il trattamento del tumore della mammella, del carcinoma della prostata e dei sarcomi pediatrici.
Tossicità
modificaLa maggior parte delle ricerche ha dimostrato che la trabectedina presenta un buon profilo di sicurezza e nella maggior parte dei pazienti è ben tollerata. In uno studio riguardante il trattamento del sarcoma, solo il 5% dei pazienti ha richiesto ospedalizzazione dovuta agli effetti collaterali del farmaco[17]. I più comuni effetti collaterali, anche se meno frequenti se confrontati agli altri chemioterapici, sono risultati essere:
- nausea
- vomito
- fatigue
Uno studio dell'European Organisation for the Research and Treatment of Cancer (EORTC) ha tuttavia messo l'accento sulla tossicità ematologica: neutropenia, trombocitopenia e anemia sono risultati i principali fattori dose-limitante[18], però rapidamente reversibili con la sospensione del farmaco. Lo stesso studio ha evidenziato altresì l'epatotossicità, come testimoniato dall'aumento delle transaminasi nel 35 – 45% dei pazienti e dalla colangite subclinica (42 – 63%), caratterizzata da un aumento della fosfatasi alcalina e/o della bilirubina. Dati simili sono pervenuti da altre ricerche[19][20] .
Note
modifica- ^ a b c M. D'Incalci, CM. Galmarini, A review of trabectedin (ET-743): a unique mechanism of action., in Mol Cancer Ther, vol. 9, n. 8, agosto 2010, pp. 2157-63, DOI:10.1158/1535-7163.MCT-10-0263, PMID 20647340.
- ^ a b E Erba, D Bergamaschi, L Bassano, G Damia, S Ronzoni, G T Faircloth, M D'Incalci, Ecteinascidin-743 (ET-743), a natural marine compound, with a unique mechanism of action, in European journal of cancer (Oxford, England: 1990), vol. 37, n. 1, 2001-01, pp. 97–105, ISSN 0959-8049, PMID 11165136.
- ^ L H Hurley, M Zewail-Foote, The antitumor agent ecteinascidin 743: characterization of its covalent DNA adducts and chemical stability, in Advances in experimental medicine and biology, vol. 500, 2001, pp. 289–299, ISSN 0065-2598, PMID 11764956.
- ^ Gregory J Aune, Takahisa Furuta, Yves Pommier, Ecteinascidin 743: a novel anticancer drug with a unique mechanism of action, in Anti-cancer drugs, vol. 13, n. 6, 2002-07, pp. 545–555, ISSN 0959-4973, PMID 12172500.
- ^ Y Takebayashi, P Pourquier, D B Zimonjic, K Nakayama, S Emmert, T Ueda, Y Urasaki, A Kanzaki, S I Akiyama, N Popescu, K H Kraemer, Y Pommier, Antiproliferative activity of ecteinascidin 743 is dependent upon transcription-coupled nucleotide-excision repair, in Nature medicine, vol. 7, n. 8, 2001-08, pp. 961–966, DOI:10.1038/91008, ISSN 1078-8956, PMID 11479630.
- ^ Daniele Grazziotin Soares, Alexandre E Escargueil, Virginie Poindessous, Alain Sarasin, Aimery de Gramont, Diego Bonatto, João Antonio Pêgas Henriques, Annette K Larsen, Replication and homologous recombination repair regulate DNA double-strand break formation by the antitumor alkylator ecteinascidin 743, in Proceedings of the National Academy of Sciences of the United States of America, vol. 104, n. 32, 7 agosto 2007, pp. 13062–13067, DOI:10.1073/pnas.0609877104, ISSN 0027-8424, PMC PMC1941813, PMID 17656556.
- ^ Kathleen W Scotto, ET-743: more than an innovative mechanism of action, in Anti-cancer drugs, 13 Suppl 1, 2002-05, pp. –3-6, ISSN 0959-4973, PMID 12173491.
- ^ M Bonfanti, E La Valle, J M Fernandez Sousa Faro, G Faircloth, G Caretti, R Mantovani, M D'Incalci, Effect of ecteinascidin-743 on the interaction between DNA binding proteins and DNA, in Anti-cancer drug design, vol. 14, n. 3, 1999-06, pp. 179–186, ISSN 0266-9536, PMID 10500494.
- ^ Debbie Friedman, Zhen Hu, E Anders Kolb, Barbara Gorfajn, Kathleen W Scotto, Ecteinascidin-743 inhibits activated but not constitutive transcription, in Cancer research, vol. 62, n. 12, 15 giugno 2002, pp. 3377–3381, ISSN 0008-5472, PMID 12067978.
- ^ Paola Allavena, Mauro Signorelli, Marcello Chieppa, Eugenio Erba, Giancarlo Bianchi, Federica Marchesi, Chiara Omero Olimpio, Claudia Bonardi, Annalisa Garbi, Andrea Lissoni, Filippo de Braud, José Jimeno, Maurizio D'Incalci, Anti-inflammatory properties of the novel antitumor agent yondelis (trabectedin): inhibition of macrophage differentiation and cytokine production, in Cancer research, vol. 65, n. 7, 1º aprile 2005, pp. 2964–2971, DOI:10.1158/0008-5472.CAN-04-4037, ISSN 0008-5472, PMID 15805300.
- ^ Giovanni Germano, Roberta Frapolli, Matteo Simone, Michele Tavecchio, Eugenio Erba, Samantha Pesce, Fabio Pasqualini, Federica Grosso, Roberta Sanfilippo, Paolo G Casali, Alessandro Gronchi, Emanuela Virdis, Eva Tarantino, Silvana Pilotti, Angela Greco, Manuela Nebuloni, Carlos Maria Galmarini, Juan Carlos Tercero, Alberto Mantovani, Maurizio D'Incalci, Paola Allavena, Antitumor and anti-inflammatory effects of trabectedin on human myxoid liposarcoma cells, in Cancer research, vol. 70, n. 6, 15 marzo 2010, pp. 2235–2244, DOI:10.1158/0008-5472.CAN-09-2335, ISSN 1538-7445, PMID 20215499.
- ^ EMA: Yondelis riassunto destinato al pubblico (PDF), su ema.europa.eu.
- ^ ORPHAN DESIGNATION OF ET-743 for the treatment of soft tissue sarcoma (PDF), su ema.europa.eu.
- ^ ORPHAN DESIGNATION OF ET-743 for the treatment of ovarian cancer (PDF), su ema.europa.eu.
- ^ NJ. Carter, SJ. Keam, Trabectedin: a review of its use in soft tissue sarcoma and ovarian cancer., in Drugs, vol. 70, n. 3, febbraio 2010, pp. 355-76, DOI:10.2165/11202860-000000000-00000, PMID 20166769.
- ^ S.Korea approves Zeltia cancer drug Yondelis | Reuters, su reuters.com (archiviato dall'url originale il 24 settembre 2015).
- ^ George D Demetri, Sant P Chawla, Margaret von Mehren, Paul Ritch, Laurence H Baker, Jean Y Blay, Kenneth R Hande, Mary L Keohan, Brian L Samuels, Scott Schuetze, Claudia Lebedinsky, Yusri A Elsayed, Miguel A Izquierdo, Javier Gómez, Youn C Park, Axel Le Cesne, Efficacy and safety of trabectedin in patients with advanced or metastatic liposarcoma or leiomyosarcoma after failure of prior anthracyclines and ifosfamide: results of a randomized phase II study of two different schedules, in Journal of clinical oncology: official journal of the American Society of Clinical Oncology, vol. 27, n. 25, 1º settembre 2009, pp. 4188–4196, DOI:10.1200/JCO.2008.21.0088, ISSN 1527-7755, PMID 19652065.
- ^ A Le Cesne, J Y Blay, I Judson, A Van Oosterom, J Verweij, J Radford, P Lorigan, S Rodenhuis, I Ray-Coquard, S Bonvalot, F Collin, J Jimeno, E Di Paola, M Van Glabbeke, O S Nielsen, Phase II study of ET-743 in advanced soft tissue sarcomas: a European Organisation for the Research and Treatment of Cancer (EORTC) soft tissue and bone sarcoma group trial, in Journal of clinical oncology: official journal of the American Society of Clinical Oncology, vol. 23, n. 3, 20 gennaio 2005, pp. 576–584, DOI:10.1200/JCO.2005.01.180, ISSN 0732-183X, PMID 15659504.
- ^ R Garcia-Carbonero, J G Supko, J Manola, M V Seiden, D Harmon, D P Ryan, M T Quigley, P Merriam, J Canniff, G Goss, U Matulonis, R G Maki, T Lopez, T A Puchalski, M A Sancho, J Gomez, C Guzman, J Jimeno, G D Demetri, Phase II and pharmacokinetic study of ecteinascidin 743 in patients with progressive sarcomas of soft tissues refractory to chemotherapy, in Journal of clinical oncology: official journal of the American Society of Clinical Oncology, vol. 22, n. 8, 15 aprile 2004, pp. 1480–1490, DOI:10.1200/JCO.2004.02.098, ISSN 0732-183X, PMID 15084621.
- ^ A Yovine, M Riofrio, J Y Blay, E Brain, J Alexandre, C Kahatt, A Taamma, J Jimeno, C Martin, Y Salhi, E Cvitkovic, J L Misset, Phase II study of ecteinascidin-743 in advanced pretreated soft tissue sarcoma patients, in Journal of clinical oncology: official journal of the American Society of Clinical Oncology, vol. 22, n. 5, 1º marzo 2004, pp. 890–899, DOI:10.1200/JCO.2004.05.210, ISSN 0732-183X, PMID 14990645.
Bibliografia
modificaRiviste
modifica- S. El-Safadi, U. Stahl; HR. Tinneberg; A. Hackethal; K. Muenstedt, Primary signet ring cell mucinous ovarian carcinoma: a case report and literature review., in Case Rep Oncol, vol. 3, n. 3, settembre 2010, pp. 451-7, DOI:10.1159/000323003, PMID 21611142.
- W. Lamm, G. Amann; T. Brodowicz, Case Report of Suspected Rhabdomyolysis during Treatment with Trabectedin in a Patient with Metastatic Leiomyosarcoma., in Case Rep Oncol, vol. 3, n. 3, settembre 2010, pp. 477-9, DOI:10.1159/000323261, PMID 21611101.
- C. Gajdos, A. Elias, Trabectedin: safety and efficacy in the treatment of advanced sarcoma., in Clin Med Insights Oncol, vol. 5, 2011, pp. 35-43, DOI:10.4137/CMO.S4907, PMID 21499557.
- PA. Cassier, A. Duret; O. Trédan; N. Carrabin; P. Méeus; I. Treilleux; JP. Guastalla; I. Ray-Coquard, New developments in treatment of ovarian carcinoma: focus on trabectedin., in Cancer Manag Res, vol. 2, 2010, pp. 233-42, DOI:10.2147/CMR.S9459, PMID 21188115.
- T. Schmitt, E. Keller; S. Dietrich; P. Wuchter; AD. Ho; G. Egerer, Trabectedin for metastatic soft tissue sarcoma: a retrospective single center analysis., in Mar Drugs, vol. 8, n. 10, 2010, pp. 2647-58, DOI:10.3390/md8102647, PMID 21116412.
- KA. Thornton, Trabectedin: the evidence for its place in therapy in the treatment of soft tissue sarcoma., in Core Evid, vol. 4, 2010, pp. 191-8, PMID 20694075.
- M. D'Incalci, CM. Galmarini, A review of trabectedin (ET-743): a unique mechanism of action., in Mol Cancer Ther, vol. 9, n. 8, agosto 2010, pp. 2157-63, DOI:10.1158/1535-7163.MCT-10-0263, PMID 20647340.
- SB. Kaye, N. Colombo; BJ. Monk; S. Tjulandin; B. Kong; M. Roy; S. Chan; E. Filipczyk-Cisarz; H. Hagberg; I. Vergote; C. Lebedinsky, Trabectedin plus pegylated liposomal doxorubicin in relapsed ovarian cancer delays third-line chemotherapy and prolongs the platinum-free interval., in Ann Oncol, vol. 22, n. 1, gennaio 2011, pp. 49-58, DOI:10.1093/annonc/mdq353, PMID 20643863.
- EJ. Soini, B. García San Andrés; T. Joensuu, Trabectedin in the treatment of metastatic soft tissue sarcoma: cost-effectiveness, cost-utility and value of information., in Ann Oncol, vol. 22, n. 1, gennaio 2011, pp. 215-23, DOI:10.1093/annonc/mdq339, PMID 20627875.
- EL. Simpson, R. Rafia; MD. Stevenson; D. Papaioannou, Trabectedin for the treatment of advanced metastatic soft tissue sarcoma., in Health Technol Assess, 14 Suppl 1, maggio 2010, pp. 63-7, DOI:10.3310/hta14Suppl1/09, PMID 20507805.
- G. Germano, R. Frapolli; M. Simone; M. Tavecchio; E. Erba; S. Pesce; F. Pasqualini; F. Grosso; R. Sanfilippo; PG. Casali; A. Gronchi, Antitumor and anti-inflammatory effects of trabectedin on human myxoid liposarcoma cells., in Cancer Res, vol. 70, n. 6, marzo 2010, pp. 2235-44, DOI:10.1158/0008-5472.CAN-09-2335, PMID 20215499.
- RA. van Waterschoot, RM. Eman; E. Wagenaar; CM. van der Kruijssen; H. Rosing; JH. Beijnen; AH. Schinkel, ABCC2, ABCC3, and ABCB1, but not CYP3A, Protect against Trabectedin-Mediated Hepatotoxicity., in Clin Cancer Res, vol. 15, n. 24, dicembre 2009, pp. 7616-7623, DOI:10.1158/1078-0432.CCR-09-2127, PMID 19996204.
Testi
modifica- (EN) Derek G. Waller, Andrew G. Renwick e Keith Hillier, Medical Pharmacology and Therapeutics, Elsevier srl, 20 ottobre 2009, pp. 565–, ISBN 978-0-7020-2991-2.
- (EN) Heinz Mehlhorn, Nature Helps...: How Plants and Other Organisms Contribute to Solve Health Problems, Springer, 29 giugno 2011, pp. 162–, ISBN 978-3-642-19381-1.
- (EN) Richard R. Barakat, Maurie Markman e Marcus Randall, Principles and Practice of Gynecologic Oncology, Lippincott Williams & Wilkins, 1º maggio 2009, pp. 498–, ISBN 978-0-7817-7845-9.
- (EN) Sotiris Missailidis, Anticancer Therapeutics, John Wiley and Sons, 13 ottobre 2008, pp. 121–, ISBN 978-0-470-69703-0.
- (EN) Gail Wilkes, Gail M Wilkes, R.N., M.S., Margaret Barton-Burke, Margaret Barton-Burke, R.N., PH.D., 2011 Oncology Nursing Drug Handbook, Jones & Bartlett Publishers, 14 dicembre 2010, pp. 319–, ISBN 978-1-4496-0013-6.
- (EN) Roland T. Skeel e Samir Khleif, Handbook of Cancer Chemotherapy, Lippincott Williams & Wilkins, 23 maggio 2011, pp. 320–, ISBN 978-1-60831-782-0.
- (ES) Hueman, M.T., Clínicas Quirúrgicas de Norteamérica 2008. Volumen 88 no 3: Sarcomas de partes blandas, Elsevier España, pp. 18–, ISBN 978-84-458-1979-1.
Collegamenti esterni
modifica- Arnaldo D'Amico, Da un mollusco farmaco anti-tumorale "Blocca le cellule immunitarie corrotte", in La Repubblica, 12 febbraio 2013. URL consultato il 12 febbraio 2013.