Zinostatina
La zinostatina (nota anche con il nome di neocarzinostatina) è un antibiotico,un alchene appartenente alla famiglia delle enediyne (ovvero composti con tripli legami per ogni lato di un doppio legame), dotato di attività antitumorale. La molecola è un polipeptide, più precisamente una apoproteina, consistente di due parti, una proteica del peso molecolare di 10.700, contenente 109 residui aminoacidici di 18 tipi differenti, e di un cromoforo, labile, di natura non proteica, con struttura biciclica, responsabile della attività biologica della sostanza.[1] Nella molecola sono presenti due ponti disolfuro tra la cisteina. L'integrità della struttura, ivi compreso il collegamento trasversale dei ponti disolfuro, è essenziale per l'espletamento dell'attività biologica.[2]
| Zinostatina | |
|---|---|
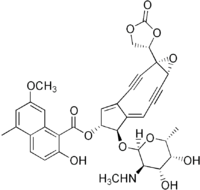 | |
| Nome IUPAC | |
| (1aS,5R,6R,6aE)-6-{[(2R,3R,4R,5R,6R)-4,5-Diidrossi-6-metil-3-(metilammino)tetraidro-2H-pyran-2-il]ossi}-1a-(2-oxo-1,3-dioxolan-4-il)-2,3,8,9-tetradeidro-1a,5,6,9a-tetraidrocyclopenta[5,6]cyclonona[1,2-b]oxiren-5-il 2-idrossi-7-methossi-5-metil-1-naphthoato | |
| Nomi alternativi | |
| Neocarzinostatina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C35H33NO12 |
| Massa molecolare (u) | 659,64 g/mol |
| Numero CAS | |
| PubChem | 57125363 |
| SMILES | CC1C(C(C(C(O1)OC2C3CC#CC4C(O4)(C#CC3=CC2OC(=O)C5=C(C=CC6=C(C=C(C=C65)OC)C)O)C7COC(=O)O7)NC)O)O |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | solubile in acqua |
| Temperatura di fusione | 260 °C |
| Dati farmacologici | |
| Categoria farmacoterapeutica | Citostatico |
| Dati farmacocinetici | |
| Escrezione | Renale |
| Indicazioni di sicurezza | |
Storia
modificaLa zinostatina è stata isolata per la prima volta da colture di Streptomyces carzinostaticus, varietà F-41, e subito studiata per la sua attività antineoplastica. L'isolamento e la successiva caratterizzazione è avvenuta per merito di Ishida nel 1965.[3][4]
Farmacodinamica
modificaIl cromoforo della molecola è un agente molto potente, in grado di danneggiare il DNA. È estremamente labile ed il ruolo dell'apoproteina è quello di proteggerlo e rilasciarlo verso il DNA bersaglio.[5] L'apertura dell'epossido, nell'ambiente riducente presente all'interno della cellula, crea le condizioni favorevoli per una ciclizzazione di Bergman, portando ad un diradicale intermedio ed infine allo sfaldamento del doppio filamento di DNA. La rottura del filamento di DNA sembra avvenire preferibilmente a livello del desossiribosio della timina. I primi studi sperimentali dimostrarono che zinostatina era altamente attiva nei confronti di vari tumori e leucemie che determinavano ascite nei topi e nei ratti, quando veniva somministrata per via intraperitoneale.[6][7][8]
Farmacocinetica
modificaDopo iniezione endovenosa, neocarzinostatina è ben assorbita e si distribuisce rapidamente nell'organismo, venendo poi rapidamente escreta nelle urine. Studi sperimentali condotti sui topi hanno evidenziato che a seguito dell'iniezione di una dose di 100 mg/kg per via endovenosa le concentrazioni più elevate si riscontravano a livello del tessuto renale con livelli decrescenti nel sangue, nei tessuti tumorali, pelle, stomaco, polmone, pancreas, timo e tessuto muscolare. In questo neocarzinostatina ricorda la distribuzione tipica della bleomicina, ad eccezione di stomaco e pancreas, dove raggiunge invece concentrazioni elevate.
Tossicità
modificaI valori della DL50 nel topo sono di 1050 mg/kg per os e di 0,96 mg/kg per via endovenosa.
Usi clinici
modificaIl composto è stato impiegato nel trattamento della leucemia e di neoplasie, incluse quelle dello stomaco e del pancreas. Un derivato della zinostatina coniugato con un polimero di stirene-acido maleico, noto con il nome di zinostatina stimalamer (SMANCS), è stato utilizzato come infusione intrarteriosa ripetuta, nel trattamento dell'epatocarcinoma.[9][10]
Chimica
modificaNeocarzinostatina, in soluzione acquosa, assorbe la radiazione ultravioletta (UV) alla lunghezza d'onda di 278 nm.
Note
modifica- ^ G. Albers-Schönberg, RS. Dewey; OD. Hensens; JM. Liesch; MA. Napier; IH. Goldberg, Neocarzinostatin: chemical characterization and partial structure of the non-protein chromophore., in Biochem Biophys Res Commun, vol. 95, n. 3, agosto 1980, pp. 1351-6, PMID 6448053.
- ^ J. Meienhofer, H. Maeda; CB. Glaser; J. Czombos; K. Kuromizu, Primary structure of neocarzinostatin, an antitumor protein., in Science, vol. 178, n. 4063, novembre 1972, pp. 875-6, PMID 4563817.
- ^ N. Ishida, K. Miyazaki; K. Kumagai; M. Rikimaru, Neocarzinostatin, an antitumor antibiotic of high molecular weight. Isolation, physiochemical properties and biological activities., in J Antibiot (Tokyo), vol. 18, marzo 1965, pp. 68-76, PMID 14326086.
- ^ H. Maeda, K. Kumagai; N. Ishida, Characterization of neocarzinostatin., in J Antibiot (Tokyo), vol. 19, n. 6, novembre 1966, pp. 253-9, PMID 6013238.
- ^ IH. Goldberg, T. Hatayama; LS. Kappen; MA. Napier, DNA as a target for a protein antibiotic: molecular basis of action., in Mol Biol Biochem Biophys, vol. 32, 1980, pp. 308-22, PMID 6449657.
- ^ K. Kumagi, Antitumor activity of carzinostatin. (Studies on the antibiotic substances from Actinomycetes. XLV)., in J Antibiot (Tokyo), vol. 15, marzo 1962, pp. 53-9, PMID 14036944.
- ^ WT. Bradner, DJ. Hutchison, Neocarzinostatin (NSC-69856): an antitumor antibiotic effective against ascitic leukemia L1210 in mice., in Cancer Chemother Rep, vol. 50, n. 1, Gen-Feb 1966, pp. 79-84, PMID 5908739.
- ^ H. Satoh, Ichimura H., Antitumor spectrum of neocarzinostatin on ascites hepatomas in rats, in Igaku no Ayumi, n. 74, 1970, pp. 499-500.
- ^ T. Okusaka, S. Okada; H. Ishii; M. Ikeda; H. Nakasuka; H. Nagahama; R. Iwata; H. Furukawa; K. Takayasu; Y. Nakanishi; M. Sakamoto, Transarterial chemotherapy with zinostatin stimalamer for hepatocellular carcinoma., in Oncology, vol. 55, n. 4, pp. 276-83, PMID 9663415.
- ^ T. Okusaka, S. Okada; H. Ueno; M. Ikeda; R. Iwata; H. Furukawa; K. Takayasu; N. Moriyama; T. Sato; K. Sato, Transcatheter arterial embolization with zinostatin stimalamer for hepatocellular carcinoma., in Oncology, vol. 62, n. 3, 2002, pp. 228-33, PMID 12065870.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su zinostatina