Utente:Grasso Luigi/sanbox1/Selenito
| Selenito | |
|---|---|
 | |
| Nome IUPAC | |
| Selenito[1][2] | |
| Nomi alternativi | |
| Ione selenito | |
| Caratteristiche generali | |
| Formula bruta o molecolare | SeO2−3 |
| Massa molecolare (u) | 126.968[3] |
| Numero CAS | Immagine_3D |
| SMILES | [O-][Se](=O)[O-] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| Frasi H | ---[4] |
| Consigli P | ---[5] |
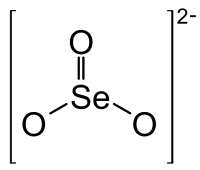
L'anione selenito è un ossoanione del selenio con formula chimica SeO2−3.I composti detti seleniti sono quelli contenenti questo ione.
In condizioni leggermente acide, si forma lo ione idrogenselenito, HSeO−3; in condizioni più acide si forma l'acido selenioso, H2SeO3. Vedi Categoria:Seleniti per una lista dei suoi composti.
Struttura modifica
Lo ione selenito ha forma piramidale e l'atomo del selenio è il picco della piramide. Le distanze tra gli atomi di selenio e ossigeno sono 1.72 A. Nella struttura dell'anione selenito, l'atomo del selenio ha un lone pairs, che funziona nei composti seleniti come ligando invisibile influenzando la loro struttura cristallina.[6][7]
Sintesi modifica
I seleniti possono essere preparati neutralizzando l'acido selenico con ossidi metallici o idrossidi. La maggior parte dei sali di selenito può essere formata riscaldando il relativo ossido di metallo con diossido di selenio, per esempio:[6][8][9][10]
- Na2O + SeO2 → Na2SeO3.
I seleniti sono utilizzati tra l'altro nei fertilizzanti e il selenito di sodio, selenito di bario nella fabbricazione del vetro.
Voci correlate modifica
Note modifica
- ^ Nomenclature of Inorganic Chemistry : IUPAC Recommendations 2005 (Red Book), Cambridge, The Royal Society of Chemistry, 2005, ISBN 978-0-85404-438-2.
- ^ (EN) PubChem Compound, CID 1090 - Compound Summary, su pubchem.ncbi.nlm.nih.gov, National Center for Biotechnology Information. URL consultato il 9 Gennaio 2019.
- ^ (EN) IUPAC Commission on Isotopic Abundances and Atomic Weights., Atomic weights of the elements 2017, su Queen Mary University of London.
- ^ Scheda del composto su ARPA
- ^ Scheda del composto su IFA-GESTIS
- ^ a b (EN) Inorganic chemistry, Academic Press, 2001, p. 583, ISBN 978-0-12-352651-9. URL consultato il 27-12-2010. Ospitato su Google ricerca libri.
- ^ (EN) Handbook of chalcogen chemistry, RSCPublishing, 2007, p. 354, ISBN 978-0-85404-366-8. URL consultato il 27-12-2010. Ospitato su Google ricerca libri.
- ^ J. E. Hoffmann & M. G. King : Selenium and Selenium Compounds, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2001 Versione web Accesso 27.12.2010
- ^ Bernd E. Langner: Selenium and Selenium Compounds Compounds, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2002 Versione web Accesso 27.12.2010
- ^ (EN) Chemistry of the Elements, 2ª ed., Butterworth Heinemann, 1992, p. 778, ISBN 0-7506-3365-4.
Altri progetti modifica
- Wikimedia Commons contiene immagini o altri file su Grasso Luigi/sanbox1/Selenito

