Anisolo
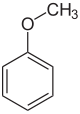
L'anisolo è un composto aromatico che presenta un metossido (CH3O-) unito all'anello aromatico del benzene.
| Anisolo | |
|---|---|
 | |
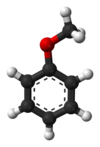 | |
| Nome IUPAC | |
| metossibenzene | |
| Nomi alternativi | |
| fenilmetiletere
fenossimetano | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C7H8O |
| Massa molecolare (u) | 108,14 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 202-876-1 |
| PubChem | 7519 |
| SMILES | COc1ccccc1 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,02 g/cm3 |
| Solubilità in acqua | 1,04 g/l[1] |
| Coefficiente di ripartizione 1-ottanolo/acqua | 2,11 |
| Temperatura di fusione | −37 °C (35 °F; 236,15 K) |
| Temperatura di ebollizione | 155 °C (428,15 K) |
| Tensione di vapore (Pa) a 25 °C K | 470 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 3700 mg/kg (topo, via orale) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 52 °C |
| Temperatura di autoignizione | 475 °C |
| Simboli di rischio chimico | |
 
| |
| attenzione | |
| Frasi H | 226 - 315 - 319 |
| Consigli P | 305+351+338 [2] |
Possiede il tipico odore e sapore dell'anice, ed è contenuto in esso.
Questo composto è principalmente sintetizzato artificialmente ed è un precursore di altri composti sintetici.
Reattività
modificaL'anisolo può subire sostituzioni elettrofile aromatiche più velocemente di quanto lo faccia il benzene, che a sua volta reagisce più velocemente del nitrobenzene. Il gruppo metossido è un gruppo orto/para orientante, ciò significa che la sostituzione avverrà preferenzialmente in una di queste tre posizioni. Il comportamento maggiormente nucleofilo dell'anisolo rispetto al benzene mostra l'influenza del gruppo metossido, che rende l'anello più ricco di elettroni.
Come esempio del suo comportamento nucleofilo, l'anisolo reagisce con l'anidride acetica producendo 4-metossiacetofenone secondo la reazione:
CH3OC6H5 + (CH3CO)2O → CH3OC6H4C(O)CH3 + CH3CO2H
Diversamente da molti acetofenoni, riflettendo comunque l'influenza del gruppo metossido, il metossiacetofenone può subire una seconda acetilazione. Per esempio, il pentasolfuro di fosforo converte l'anisolo nel reagente di Lawesson.
Il legame etereo è molto stabile, ma il gruppo metile può essere rimosso con acido iodidrico:
CH3OC6H5 + HI → HOC6H5 + CH3I
Sintesi
modificaL'anisolo è preparato tramite la sintesi di Williamson, facendo reagire fenossido di sodio con bromometano e relativi agenti metilanti[3]:
Usi
modificaL'anisolo è un precursore per profumi, ferormoni di insetti e farmaci.[4] Per esempio, l'anetolo sintetico è preparato a partire dall'anisolo.
Sicurezza
modificaL'anisolo è relativamente non tossico, con un LD50 di 3700 mg/kg nei topi.[5] Il suo principale pericolo è la sua infiammabilità.[5][6]
Note
modifica- ^ http://www.hmdb.ca/metabolites/HMDB33895
- ^ Sigma Aldrich; rev. del 04.07.2013
- ^ http://www.orgsyn.org/demo.aspx?prep=cv1p0058, su orgsyn.org. URL consultato il 4 marzo 2017.
- ^ (EN) Helmut Fiege, Heinz-Werner Voges e Toshikazu Hamamoto, Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH Verlag GmbH & Co. KGaA, 1º gennaio 2000, DOI:10.1002/14356007.a19_313, ISBN 9783527306732. URL consultato il 4 marzo 2017.
- ^ a b Mallinckrodt Baker, Inc., Material Safe Data Sheet of anisole (PDF) (archiviato dall'url originale il 1º luglio 2010).
- ^ ICSC 1014 - ANISOLE, su inchem.org. URL consultato il 4 marzo 2017.
Altri progetti
modifica- Wikizionario contiene il lemma di dizionario «anisolo»
- Wikimedia Commons contiene immagini o altri file su anisolo
Collegamenti esterni
modifica- (EN) anisole, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | GND (DE) 4319568-4 |
|---|