Permetrina
La permetrina (C21H20Cl2O3) è una sostanza attiva antiparassitaria utilizzata per i presidi medico-chirurgici e come insetticida. Appartiene alla famiglia dei piretroidi ed agisce come neurotossina.
| Permetrina | |
|---|---|
 | |
 | |
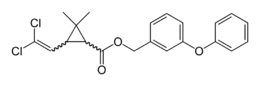
| Nome IUPAC | |
| 3-fenossibenzil- (1RS)-cis,trans-3-(2,2-diclorovinile)-2,2- dimetilciclopropanocarbossilato | |
| Nomi alternativi | |
| permetrina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C21H20Cl2O3 |
| Aspetto | cristalli incolori |
| Numero CAS | |
| Numero EINECS | 258-067-9 |
| PubChem | 40326 |
| DrugBank | DBDB04930 |
| SMILES | CC1(C(C1C(=O)OCC2=CC(=CC=C2)OC3=CC=CC=C3)C=C(Cl)Cl)C |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,19 |
| Temperatura di fusione | 34 °C (307 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| attenzione | |
| Frasi H | 302 - 317 - 332 - 410 |
| Consigli P | 273 - 280 - 501 [1][2] |
Principio di funzionamento
modificaIl sito primario d'azione di tutte e due le classi è a livello dei canali del sodio a livello della membrana cellulare degli elementi eccitabili. Dopo il passaggio di un potenziale d'azione nelle cellule eccitabili del tessuto nervoso e di quello muscolare, le piretrine ed i piretroidi bloccano l'apertura di una certa percentuale dei canali di membrana per il sodio. Questi agenti vengono quindi detti bloccanti dell'apertura dei canali.
Normalmente, dopo il passaggio di un potenziale d'azione, l'iniziale flusso di ioni sodio verso l'interno della cellula viene rapidamente ridotto. In presenza di piretrine e piretroidi, invece, si ha il perdurare di un certo afflusso di sodio. Il continuo afflusso di ioni sodio determina dopo il potenziale d'azione primario un prolungamento della corrente. Questo, a sua volta, è causa di ripetute scariche delle cellule eccitabili. Il persistere di tale depolarizzazione inibisce la propagazione di ulteriori potenziali d'azione, provocando, quindi, la paralisi nervosa.[3]
Utilizzi
modificaIn agricoltura è utilizzata principalmente per disinfestare le colture di cotone, frumento, mais e erba medica, mentre negli allevamenti trova utilizzo nell'uccidere i parassiti dei polli. Il suo utilizzo è controverso dal momento che, essendo un veleno ad ampio spettro, uccide indiscriminatamente le varie specie di insetti comprese quelle non dannose come le api.
Si utilizza per eliminare parassiti umani come il pidocchio e la scabbia e per tenere sotto controllo scarafaggi, termiti, tarli, formiche sia in ambito domestico che industriale. Permetrina di grado farmaceutico è prodotta commercialmente da aziende come VAV Life Sciences, Dow Chemicals etc.
La permetrina elimina acari e zecche al semplice contatto con tessuti trattati. Secondo gli studi del Connecticut Department of Public Health ha una bassa tossicità per i mammiferi, l'assorbimento attraverso la pelle è limitato e reazioni allergiche sono rare.[4] Viene, quindi, utilizzata anche sui cani per eliminare gli stessi parassiti e per tenere lontano zanzare e pappataci responsabili della trasmissione della leishmaniosi. I prodotti "spot-on" contenenti permetrina da utilizzare sui cani, garantiscono la lontananza di zanzare e pappataci per solo 2 settimane, quindi vanno applicati più spesso durante i mesi primaverili ed estivi.[senza fonte]
La permetrina non va assolutamente utilizzata sui gatti[5], in quanto ne può provocare facilmente la morte anche attraverso le vie aeree o per contatto indiretto (per esempio coricandosi nella cuccia di un animale trattato). Questo perché i gatti non sono dotati di glicosidasi[5], degli enzimi necessari ad eliminare dal loro organismo la molecola di permetrina, che verso di loro agisce come un vero e proprio veleno.
Tossicità
modificaÈ altamente tossica per api, pesci e invertebrati acquatici[6] a causa della sua azione di disfacimento dei canali del sodio. Ha gravi effetti sui gatti causando gravi disturbi del sistema nervoso.
Nel dicembre del 2000 la Commissione europea ha ritirato l'approvazione come insetticida in agricoltura e imposto il ritiro dal commercio in breve tempo.[7] Nel 2024 continua a essere approvato come insetticida per uso non fitosanitario.[8][9]
Anche se in commercio prevalgono le formulazioni contenenti gli isomeri cis-trans in rapporto 1:3, le formulazioni più attive, almeno nei test di laboratorio, sono risultate quelle aventi gli isomeri cis-trans in rapporto 2:3.
Invertebrati acquatici
modificaRicerche con anfipodi di acqua dolce indicano che la presenza di permetrina nei sedimenti acquatici può inibirne la crescita a livelli di 44-73 ng*g -1 sedimento (Amweg et al. 2005).
Crustacea
modificaTossicità elevata per la maggior parte dei crostacei (PAN Database). Questa sostanza induce l’adesione di sedimenti, alghe, batteri e frammenti silicei sulle appendici di Daphnia magna. Analogo effetto ha la cipermetrina. LC 50 48-ore Daphnia (forme giovanili) = 0,2-0.6 µg*l -1 .
Mollusca
modificaTossicità variabile che può essere elevata per alcune lumache di acqua dolce (ad es. LC 50 Lymnaea acuminata = 542.5 µg*l -1 .
Insecta
modificaDa Molto ad Estremamente tossico per la maggior parte degli insetti. Nelle api oltre all'alta tossicità orale e per contatto determina significativi effetti cronici: esposizioni subletali alla permetrina (piretroide) riducono le capacità di apprendimento degli odori (Taylor et al. 1987; Decourtye & Pham-Delegue, 2002).
In Francia gli allevamenti di bovini e ovini vengono trattati con prodotti polverizzati a base di permetrina, per combattere mosche e zanzare vettori del tanto temuto "morbo della lingua blu". Sembrerebbe che sia questa un’altra delle ragioni che spiegano l’improvvisa e massiva morìa negli alveari delle zone colpite da questa patologia animale. A dare l'allarme la Commissione Nazionale per l'apicoltura francese. Campioni di api morte, inviati ai laboratori del Centro Nazionale per la Ricerca Scientifica, sono infatti risultati positivi al piretroide che è risultato presente in dosi letali anche nei campionamenti ambientali svolti nei pressi degli allevamenti e persino sui mezzi di trasporto degli animali. Le perdite negli apiari hanno raggiunto dal 50 all'80% delle colonie. Anche apicoltori dell' Aude, dei Pirenei Orientali, degli Alti Pirenei, dell’ Alta Vienne e dell' Aveyron hanno segnalato perdite importanti e sintomi identici. Numerosi esperti ed enti contestano l’utilità e l'efficacia di tale lotta insetticida. Gli apicoltori hanno chiesto al Ministero dell'Agricoltura francese di modificare il decreto del 4 novembre 2008 relativo alla disinfezione obbligatoria e d’intervenire presso la Commissione Europea per ottenere la modifica della Direttiva europea 2000/75, che stabilisce le disposizioni relative alla lotta ed eradicazione della febbre catarrale degli ovini. Prove di laboratorio ne hanno dimostrato l'effetto sinergico, molto spiccato, quando viene impiegata con gli esteri fosforici e con i piretroidi di ultima generazione (eccezione fatta per la Deltametrina).
Pisces
modificaLa tossicità varia da debole ad estrema. Altamente tossica per alcune specie di pesci di acqua marina e dolce (US Environmental Protection Agency, 2006). È altamente tossica per cefali (LC 50 Mugil cephalus 5.50 µg*l -1 ), persici (LC 50 Micropterus salmoides 8.50 µg*l -1 ), salmerini (LC 50 3.58 µg*l -1), Trota iridea (LC 50 Oncorhynchus mykiss 19 µg*l -1 ) (PAN Database). Tende ad accumularsi nell’organismo e determina variazioni nel comportamento e alterazioni biochimiche. Studi di proteomica su Pimephales promelas hanno portato alla constatazione che questa sostanza è in grado, in proporzioni subletali (7.5 µg*l -1 ), di alterare l’espressione di 24 proteine (Biales et al. , 2011). Nella maggior parte delle specie testate la Tossicità acuta rientra nella Categoria 1 MOLTO TOSSICO PER LA VITA ACQUATICA.
Amphibia
modificaLa tossicità acuta è molto variabile, da debole per i rospi a estremamente alta per alcune specie di rana.
Aves
modificaLa tossicità acuta è moderata (DL 50 pollo > 3000 mg*kg -1 ), ma livelli molto bassi di permetrina (0.1 ppm per 3-6 settimane) nella dieta delle Galline ( Gallus gallus domesticus ) hanno portato alla soppressione del sistema immunitario.
Mammalia
modificaLa Permetrina è stata largamente utilizzata come antiparassitario per uso esterno (collari, polveri, spray) per cani e gatti (NTPN, 1997). Nei cani, generalmente, i piretroidi sono ben tollerati, così come i ratti e i topi, mentre di frequente i gatti esposti manifestano i sintomi dell’intossicazione. Veterinari della VPIS (US Veterinary Poisons Information Service) hanno osservato che il 96.9% dei gatti esposti a formulazioni della sostanza mostravano i sintomi tipici dell’avvelenamento (Sutton et al. 2007). Nell’87.8% dei casi compariva ipereccitabilità, tremori muscolari o convulsioni tonico-cloniche lievi, difficoltà di deambulazione e nel mantenimento della stazione quadrupedale, ipersalivazione, vomito, diarrea, dispnea, midriasi. La Permetrina causa sul coniglio irritazioni di media entità sia su pelle integra che abrasa. Può anche causare congiuntiviti quando viene in contatto con gli occhi. Inibisce la proliferazione delle cellule estrogeno-sensibili (Kim et al. , 2006: McCarthy et al. , 2004).[6]
Homo sapiens
modificaPer quanto riguarda gli uomini un’associazione positiva statisticamente significativa è stata osservata con il mieloma. Il rischio relativo era aumentato di oltre 5 volte nei soggetti che erano entrati ripetutamente in contatto con la sostanza per motivi professionali. Considerato potenziale interferente endocrino dall’Unione Europea. Insieme al DEET è stata inclusa tra gli agenti neurotossici che potrebbero aver avuto un ruolo significativo nei disordini neurovegetativi dei veterani della Guerra del Golfo del 1991 (Abou-Donia et al. , 1996; Institute of Medicine, 1995). Era, infatti, largamente usata per la protezione del personale contro gli insetti portatori di eventuali malattie.[6]
Note
modifica- ^ Sigma Aldrich; rev. del 09.01.2012
- ^ Smaltire presso impianti autorizzati.
- ^ Vijverberg HPM, de Weille JR:The interaction of pyrethroids with voltage-dependent Na channels,Neurotoxicology 6:23-34, 1985
- ^ Department of Public Health Archiviato il 12 settembre 2005 in Internet Archive.
- ^ a b (EN) Deltamethrin safety, su parasitipedia.net. URL consultato il 2 settembre 2021.
- ^ a b c Impatto sugli ecosistemi e sugli esseri viventi delle sostanze sintetiche utilizzati nella profilassi anti-zanzara, su isprambiente.gov.it. URL consultato il 7 settembre 2019.
- ^ Decisione 2000/817/CE, su eur-lex.europa.eu. URL consultato il 20 marzo 2024 (archiviato il 20 marzo 2024).
- ^ Permethrin - Substance Information - ECHA [Permetrina - Informazioni sulla sostanza - ECHA], su echa.europa.eu. URL consultato il 20 marzo 2024 (archiviato il 20 marzo 2024).
- ^ (EN) Permethrin - Information on biocides - ECHA [Permetrina - Informazioni sui biocidi - ECHA], su echa.europa.eu. URL consultato il 20 marzo 2024 (archiviato il 20 marzo 2024).
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su Permetrina
Collegamenti esterni
modifica- (EN) permethrin, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.