Cicloesano
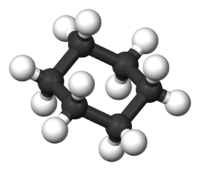
Il cicloesano è un cicloalcano, ossia un idrocarburo privo di doppi e tripli legami C-C il cui scheletro di atomi di carbonio è chiuso ad anello, per l'esattezza un anello composto da sei atomi, ciascuno dei quali lega a sé due atomi di idrogeno, la cui formula molecolare è quindi C6H12.
| Cicloesano | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | |
| cicloesano | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H12 |
| Massa molecolare (u) | 84,16 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 203-806-2 |
| PubChem | 8078 |
| SMILES | C1CCCCC1 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,78 |
| Indice di rifrazione | 1,4264 |
| Solubilità in acqua | 0,055 g/l a 293 K |
| Temperatura di fusione | 6 °C (279 K) |
| Temperatura di ebollizione | 81 °C (354 K) |
| ΔebH0 (kJ·mol−1) | 31,3 |
| Tensione di vapore (Pa) a 293 K | 10300 |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −156,4 |
| C0p,m(J·K−1mol−1) | 154,9 |
| Indicazioni di sicurezza | |
| Punto di fiamma | −18 °C (255 K) |
| Limiti di esplosione | 1,2 - 8,3% vol. |
| Temperatura di autoignizione | 260 °C (533 K) |
| Simboli di rischio chimico | |
   
| |
| pericolo | |
| Frasi H | 225 - 304 - 315 - 336 - 410 |
| Consigli P | 210 - 240 - 273 - 301+310 - 331 - 403+235 [1] |
A temperatura ambiente è un liquido incolore dal lieve odore tipico degli idrocarburi. È infiammabile e nocivo per inalazione e contatto con la pelle.
Conformazione
modificaBenché per comodità sia rappresentata da un esagono regolare, la molecola del cicloesano non è planare, dal momento che gli atomi di carbonio hanno ibridazione sp3, tetraedrica in cui l'angolo tra due legami è di 109,5°. La molecola del cicloesano tende pertanto ad assumere una forma piegata detta a sedia, individuata da Odd Hassel, che per questa ricerca ricevette un Premio Nobel per la chimica.
Nella conformazione a sedia, la più stabile, 6 dei 12 atomi di idrogeno sono in posizione assiale, ovvero i loro legami C-H sono tra loro paralleli e perpendicolari al piano medio della molecola, gli altri 6 sono in posizione equatoriale, ovvero si protendono verso l'esterno, inclinati alternativamente al di sopra e al di sotto del piano medio della molecola.
A temperatura ambiente le conformazioni si interconvertono rapidamente le une nelle altre passando da una conformazione a sedia all'altra ad essa speculare attraverso le conformazioni twist e a barca.
Il passaggio da una conformazione a sedia all'altra scambia di posto gli idrogeni: quelli in posizione assiale si ritrovano in posizione equatoriale e viceversa.
Quando al posto degli idrogeni vi sono dei gruppi sostituenti, la forma a sedia più stabile è quella che lascia i sostituenti più ingombranti in posizione equatoriale; in questo modo viene minimizzato l'ingombro sterico della molecola. Un'importante eccezione consiste nell'effetto anomerico quando vi sono eteroatomi all'interno dell'anello.
Produzione
modificaIl cicloesano si ottiene per distillazione del petrolio, ma in maggiore quantità per reforming catalitico di idrocarburi e per idrogenazione catalitica del benzene, tipicamente con Nichel Raney.
Utilizzi
modificaTrova principalmente impiego in chimica industriale come solvente: la produzione di polietilene si basa su reazione di polimerizzazione in fase liquida che usa il cicloesano come solvente veicolante. Il cicloesano si usa anche come materia prima per la produzione del nylon 6,6, derivato dell'acido adipico con l'esametilendiammina. Proprio quest'ultima si ottiene per pirolisi ammoniacale del cicloesano. Il suo mono-metil derivato è ampiamente usato come solvente dei cancellini liquidi per cancelleria.
Note
modifica- ^ scheda del cicloesano su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
Bibliografia
modifica- (EN) Klaus Weissermel, Hans-Jürgen Arpe, Charlet R. Lindley, Industrial organic chemistry, 4ª ed., Wiley-VCH, 2003, pp. 347-349, ISBN 3-527-30578-5.
Altri progetti
modifica- Wikizionario contiene il lemma di dizionario «cicloesano»
- Wikimedia Commons contiene immagini o altri file sul cicloesano
Collegamenti esterni
modifica- (EN) cyclohexane, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh85035082 · GND (DE) 4148544-0 · J9U (EN, HE) 987007538314605171 · NDL (EN, JA) 00576637 |
|---|