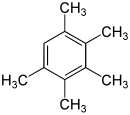
Pentametilbenzene
Il pentametilbenzene è un idrocarburo aromatico di formula C11H16. Strutturalmente è considerabile come una molecola di benzene dove cinque atomi di idrogeno sull'anello aromatico sono stati sostituiti con altrettanti gruppi metilici -CH3. In condizioni standard appare come un solido cristallino di colore beige insolubile in acqua. Il pentametilbenzene è poco utilizzato a livello industriale e la sua area di interesse è sostanzialmente limitata all'ambito della ricerca chimica. La molecola risulta instabile a contatto con sostanze fortemente ossidanti, è pertanto buona norma conservare il composto sotto vuoto in un luogo fresco, asciutto e ben ventilato[2].
| Pentametilbenzene | |
|---|---|
| Nome IUPAC | |
| 1,2,3,4,5-pentametilbenzene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C11H16 |
| Massa molecolare (u) | 148,247 |
| Aspetto | solido cristallino beige |
| Numero CAS | |
| Numero EINECS | 211-837-8 |
| PubChem | 12784 |
| SMILES | CC1=CC(=C(C(=C1C)C)C)C |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,917 a 25 °C |
| Solubilità in acqua | 15,5 mg/L |
| Coefficiente di ripartizione 1-ottanolo/acqua | 4,56 |
| Temperatura di fusione | 51 °C |
| ΔfusH0 (kJ·mol−1) | 10,67 |
| ΔfusS0 (J·K−1mol−1) | 32,5 |
| Temperatura di ebollizione | 232 °C |
| Tensione di vapore (Pa) a 293,15 K | 4,6394 |
| Proprietà termochimiche | |
| C0p,m(J·K−1mol−1) | 210,5 a 25 °C |
| Indicazioni di sicurezza | |
| Punto di fiamma | 91 ° (vaso chiuso) |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 228 - 315 - 319 - 335 |
| Consigli P | 210 - 261 - 305+351+338 [1] |
Sintesi
modificaIl pentametilbenzene può essere ottenuto per metilazione in ambiente anidro dell'1,4-xilene con clorometano, in presenza di cloruro di alluminio con funzione di catalizzatore[3]:
- + 3CH3Cl → + 3HCl
Reattività
modificaIl pentametilbenzene, reagendo in ambiente anidro con clorometano ed in presenza di cloruro di alluminio come catalizzatore, può dare la formazione di esametilbenzene[3]:
Trattasi questo del medesimo meccanismo di reazione utilizzato per la sintesi del pentametilbenzene. Tale reazione può essere considerata come un "proseguimento" del processo di sintesi in seguito all'aggiunta di un'ulteriore mole di clorometano.
Note
modifica- ^ Pentametilbenzene - scheda di dati di sicurezza (PDF), su sigma-aldrich.com, Sigma-Aldrich. URL consultato il 24 dicembre 2016.
- ^ (EN) Pentamethylbenzene, su alfa.com, Alfa Aesar. URL consultato il 24 dicembre 2016.
- ^ a b (EN) Lee Irvin Smith, Durene, in Organic Syntheses, vol. 10, n. 32, John Wiley & Sons, 1930, DOI:10.15227/orgsyn.010.0032, ISSN 0078-6209. URL consultato il 24 dicembre 2016.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su pentametilbenzene