Surrene
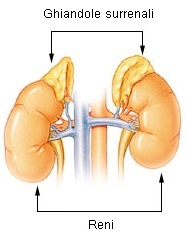
Il surrene (o ghiandola surrenale) è un organo di tutti i vertebrati composto da due ghiandole ad attività endocrina, esse sono più o meno diverse a seconda dell'apparato endocrinale animale a cui si fa riferimento. Queste ghiandole endocrine sono in grado di produrre una varietà di ormoni, tra cui l'adrenalina e gli steroidi aldosterone e cortisolo.[1][2] Esse sono posizionate sopra i reni. Ogni ghiandola possiede una parte corticale esterna, deputata alla produzione di ormoni steroidei, e una parte midollare interna. La corticale surrenale è divisa in tre zone: zona glomerulare, zona fascicolata e zona reticulata.[3]
| Surrene | |
|---|---|
 | |
 | |
| Anatomia del Gray | (EN) Pagina 1278 e (EN) Pagina 178 |
| Sistema | Sistema endocrino |
| Arteria | arteria surrenale superiore, arteria surrenale media e arteria surrenale inferiore |
| Vena | vena surrenale |
| Linfatici | linfonodi lombari |
| Identificatori | |
| MeSH | A06.300.071 |
| TA | A11.5.00.001 |
| FMA | 9604 |
La corticale surrenale produce tre tipi principali di ormoni steroidei: mineralcorticoidi, glucocorticoidi e androgeni. I mineralcorticoidi (come l'aldosterone) prodotti nella zona glomerulare contribuiscono nella regolazione della pressione sanguigna e dell'equilibrio elettrolitico. I glucocorticoidi (cortisolo e corticosterone) vengono sintetizzati nella zona fascicolata e le loro funzioni comprendono la regolazione del metabolismo e la soppressione del sistema immunitario. Lo strato più interno della corteccia, la zona reticulata, produce androgeni che vengono convertiti in ormoni sessuali completamente funzionali nelle gonadi e in altri organi bersaglio.[4] La produzione di ormoni steroidei si chiama steroidogenesi e comporta diverse reazioni e processi che avvengono nelle cellule corticali.[5] La parte midollare produce le catecolamine adrenalina e noradrenalina che servono per avere una risposta rapida di tutto l'organismo nelle situazioni di stress.[4]
Disfunzioni delle ghiandole surrenali comportano numerose malattie endocrine. Ad esempio, la sovrapproduzione di cortisolo porta alla sindrome di Cushing, mentre una produzione insufficiente è associata alla malattia di Addison. L'iperplasia surrenale congenita è una malattia genetica prodotta dalla disregolazione dei meccanismi di controllo endocrino.[4][6] Una varietà di tumori può derivare dal tessuto surrenalico e vengono comunemente diagnosticati osservando immagini biomediche ottenute nella ricerca di altre malattie.[7]
Anatomia comparata modifica
Pesci modifica
Nei gruppi tassonomici riconducibili ai pesci le ghiandole surrenali si posizionano variamente: nei condroitti, i noduli tissutali midollari si dispongono dispersi lungo il corpo in senso sagittale, e la porzione corticale viene di solito a trovarsi, condensata, a livello renale la parte corticale si trova in posizione più cefalica e nodulare, o avvolge le vene cardinali; la parte midollare può essere separata o inglobata nei noduli corticali.
Anfibi modifica
Negli Anuri, coesistono oltre alle due componenti midollari e corticali, le cellule di Stilling, a funzione di regolazione osmotica
Negli Anfibi, i due tessuti si uniscono a formare cordoni situati sulla superficie ventrale del rene.
Rettili modifica
Uccelli modifica
Mammiferi modifica
Anatomia umana modifica
Anatomia macroscopica modifica
Dal punto di vista anatomico, il surrene è un organo pari posizionato a livello dell'ultima vertebra toracica (T12) ed è irrorato da tre gruppi di arterie surrenali, superiori, medie e inferiori. Di forma triangolare, è posizionato nei pressi della sommità del rene, come dice il nome, ma da esso è clivato per mezzo di tessuto adiposo. Il surrene di sinistra è localizzato antero-medialmente e non cranialmente al polo superiore del rene sinistro, mentre a destra il surrene è subito al di sopra del polo renale, posteriormente alla vena cava inferiore.
Anatomia microscopica modifica
Ciascuna ghiandola surrenale consta di due organi strutturalmente e funzionalmente diversi. In modo simile all'ipofisi, la ghiandola surrenale è formata da una parte ghiandolare (corteccia) e da una parte di tessuto nervoso (midollare). La sostanza midollare è situata al centro, ed è avvolta dalla sostanza corticale che contiene tre diverse zone cellulari.
Parte corticale modifica
La corteccia è suddivisa, proseguendo dalla capsula verso la midollare, in:
- Zona glomerulare
La zona glomerulare deve il suo nome alla particolare organizzazione del tessuto ghiandolare in cordoni cellulari avvolti su sé stessi a formare strutture arrotondate ("glomeruli"). I mineralcorticoidi, soprattutto aldosterone, sono prodotti nella zona più esterna della corteccia. Come indica il loro nome, i mineralcorticoidi sono importanti per la regolazione del contenuto minerale (ossia dei sali) del sangue, in modo particolare della concentrazione degli ioni sodio e potassio. Il loro bersaglio è rappresentato dai tubuli renali che riassorbono in modo selettivo i minerali oppure lasciano che siano eliminati dall'organismo con l'urina. Quando il livello ematico dell'aldosterone aumenta, le cellule dei tubuli renali trattengono il sodio e fanno perdere potassio con le urine.
Dal momento che l'acqua segue il sodio che viene riassorbito, i mineralcorticoidi intervengono nel regolare anche il volume dal sangue (volemia) oltre che l'equilibrio elettrolitico dei fluidi corporei. Il rilascio di aldosterone è stimolato da fattori umorali come basse concentrazioni di ioni sodio o elevate concentrazioni di ioni potassio nel sangue e, in minor misura, dell'ormone adrenocorticotropo (ACTH). La renina, un enzima prodotto dai reni quando la pressione sanguigna si abbassa, provoca il rilascio di aldosterone mediante l'innesco di una serie di reazioni che portano alla formazione di angiotensina II, un potente stimolatore del rilascio di aldosterone. Il peptide natriuretico atriale, prodotto dal cuore, inibisce il rilascio di aldosterone, con il risultato di ridurre il volume del sangue e quindi la pressione sanguigna.
- Zona fascicolata
Ha cellule disposte a cordoni paralleli radiali. La zona corticale intermedia produce glucocorticoidi, il cortisolo. I glucocorticoidi favoriscono il normale metabolismo cellulare e aumentano le resistenze organiche nei lavori di lunga durata, sostanzialmente aumentando la glicemia. Quando i livelli ematici dei glucocorticoidi sono elevati, i grassi e anche le proteine sono demoliti all'interno delle cellule e convertiti in glucosio, che viene rilasciato nel sangue. Per questo motivo i glucocorticoidi sono considerati ormoni iperglicemizzanti. I glucocorticoidi, inoltre, controllano la maggior parte degli effetti spiacevoli dell'infiammazione riducendo l'edema e inibendo le prostaglandine, molecole responsabili dell'insorgenza del dolore. Per le loro proprietà antinfiammatorie, i glucocorticoidi sono spesso prescritti come farmaci ai pazienti affetti da artrite reumatoide. I glucocorticoidi sono rilasciati dalla corteccia surrenale in risposta all'aumento dei livelli ematici di ACTH.
- Zona reticolare (o, meno comunemente, zona reticolata)
La zona reticolata produce in entrambi i sessi, per tutta la vita, quantità relativamente piccole di ormoni sessuali sia maschili sia femminili; va però precisato che la zona interna della corteccia produce prevalentemente androgeni (ormoni sessuali maschili) e solo piccole quantità di estrogeni (ormoni sessuali femminili).
Parte midollare modifica
La midollare del surrene, come il lobo posteriore dell'ipofisi, è di origine nervosa. Quando i neuroni del sistema nervoso simpatico stimolano la midollare, le sue cellule rilasciano nel circolo sanguigno due ormoni chimicamente simili:
- adrenalina, detta anche epinefrina
- noradrenalina (norepinefrina)
Questi ormoni sono complessivamente denominati catecolamine.
La midollare comprende anche cellule parenchimali dette cellule cromaffini.
Dal momento che anche la maggior parte dei neuroni simpatici gangliari rilasciano noradrenalina come neurotrasmettitore, la midollare del surrene è spesso considerata come un ganglio del sistema nervoso simpatico dislocato dentro un organo endocrino (praticamente un'appendice del cervello distanziatasi da esso nel corso dell'evoluzione). In condizioni di stress fisico o psichico, è il sistema nervoso simpatico a mettere in atto la risposta "lotta o fuga" per fronteggiare la situazione di stress, e il principale organo stimolatore è la midollare del surrene, che pompa letteralmente i suoi ormoni nel circolo sanguigno per potenziare e prolungare gli effetti dei neurotrasmettitori prodotti dal sistema nervoso simpatico.
Le catecolamine:
- aumentano la frequenza cardiaca
- aumentano la pressione sanguigna
- aumentano i livelli di glucosio ematico
- dilatano i piccoli bronchi dei polmoni
Quindi determinano una serie di eventi destinata ad aumentare la quantità di ossigeno e di glucosio nel sangue e ad accelerare la circolazione sanguigna soprattutto negli organi più direttamente coinvolti nello stress: encefalo, muscoli e cuore. Ne consegue che l'organismo acquisisce maggiore capacità di affrontare un evento stressante improvviso, come dover affrontare una lotta o l'inizio di un processo infiammatorio, e viene anche allertato per acuire la capacità di ragionare. In sintesi, le catecolamine della midollare del surrene mettono l'organismo in condizioni di fronteggiare una situazione altamente stressante improvvisa o di breve durata, e inducono il cosiddetto periodo di allarme nella risposta allo stress.
Al contrario, i glucocorticoidi prodotti dalla corticale del surrene sono più importanti nel sostenere l'organismo a fronteggiare situazioni stressanti prolungate o continue, come la morte di un familiare o un importante intervento chirurgico. I glucocorticoidi agiscono soprattutto durante il periodo di resistenza nella risposta allo stress. Se riescono a proteggere l'organismo, il problema alla fine si risolverà senza postumi permanenti del corpo, ma se lo stress persiste per lungo tempo, la corteccia surrenale semplicemente può esaurirsi, il che di solito porta alla morte.
Patologia modifica
La normale funzione della ghiandola surrenale può essere compromessa da alcune condizioni patologiche come infezioni, tumori, malattie genetiche e malattie autoimmuni, o come effetto collaterale di terapie mediche. Questi disturbi colpiscono direttamente la ghiandola (come le infezioni o le malattie autoimmuni) o come risultato della disregolazione della produzione ormonale (come in alcuni tipi di sindrome di Cushing) che porta ad un eccesso o ad una insufficienza di ormoni surrenali e dei sintomi correlati a ciò.
Sovrapproduzione di corticosteroidi modifica
Sindrome di Cushing modifica
La sindrome di Cushing è la manifestazione di un eccesso di glucocorticoidi. Può essere causata da un trattamento prolungato con gli stessi glucocorticoidi o da una patologia sottostante che comporta alterazioni nell'asse ipotalamo-ipofisi-surrene o nella produzione di cortisolo. Le cause possono essere ulteriormente classificate in ACTH-dipendenti o ACTH-indipendenti. La causa più comune della sindrome di Cushing endogena è un adenoma pituitario che comporta una produzione eccessiva di ACTH. La malattia produce un'ampia varietà di segni e sintomi che includono obesità, diabete, aumento della pressione sanguigna, eccessiva peluria del corpo (irsutismo), osteoporosi, depressione e, più distintamente, smagliature nella pelle causate dal suo progressivo assottigliamento.[4][6]
Aldosteronismo primario modifica
Quando la zona glomerulosa produce aldosterone in eccesso si viene ad instaurare un iperaldosteronismo primario. Le cause di questa condizione sono l'iperplasia bilaterale (eccessiva crescita dei tessuti) delle ghiandole o adenomi che producono aldosterone (una condizione chiamata sindrome di Conn). L'aldosteronismo primario produce ipertensione e squilibrio elettrolitico, aumentando la diminuzione di potassio e la ritenzione di sodio.[6]
Insufficienza surrenalica modifica
L'insufficienza surrenalica (carenza di glucocorticoidi) si verifica in circa 5 persone su 10.000 nella popolazione generale.[6] Le malattie classificate come insufficienza surrenalica primaria (compresa la malattia di Addison e le cause genetiche) colpiscono direttamente la corticale surrenale. Se un problema che interessa l'asse ipotalamo-ipofisi-surrene sorge fuori dalla ghiandola, si tratta di un'insufficienza surrenalica secondaria.
Malattia di Addison modifica
Con il termine "malattia di Addison" ci si riferisce all'ipoadrenalismo primario, che è una carenza nella produzione di glucocorticoidi e mineralcorticoidi da parte della ghiandola surrenale. Nel mondo occidentale, la malattia di Addison è più comunemente una condizione autoimmune in cui l'organismo produce anticorpi contro le cellule della corticale surrenale. In tutto il mondo, la malattia è più frequentemente causata da un'infezione, in particolare a seguito della tubercolosi. Una caratteristica distintiva della malattia di Addison è l'iperpigmentazione della pelle, che si presenta con altri sintomi non specifici come la fatica.[4]
Una complicazione osservata nella malattia di Addison non trattata e in altri tipi di insufficienza surrenalica primaria è la crisi surrenalica, un'emergenza medica in cui bassi livelli di glucocorticoidi e mineralcorticoidi determinano uno shock ipovolemico e sintomi come vomito e febbre. Una crisi surrenalica può portare progressivamente allo stupor e al coma.[4] Il trattamento di questa condizione implica iniezioni di idrocortisone.[8]
Insufficienza surrenalica secondaria modifica
Nell'insufficienza surrenalica secondaria, una disfunzione dell'asse ipotalamo-ipofisi-surrene porta a una diminuzione della stimolazione della corticale surrenale. Oltre alla soppressione dell'asse mediante terapia con glucocorticoidi, la causa più comune dell'insufficienza surrenalica secondaria sono i tumori che influenzano la produzione di ormone adrenocorticotropo (ACTH) da parte della ghiandola pituitaria.[6] Questo tipo di insufficienza surrenalica di solito non influisce sulla produzione di mineralcorticoidi, che sono invece regolati dal sistema renina-angiotensina-aldosterone.[4]
Iperplasia surrenale congenita modifica
L'iperplasia surrenale congenita è una malattia congenita in cui le mutazioni degli enzimi che producono ormoni steroidei determinano una carenza di glucocorticoidi e un malfunzionamento del circuito di feedback negativo dell'asse ipotalamo-ipofisi-surrene. In tale asse, il cortisolo (un glucocorticoide) inibisce il rilascio di CRH e ACTH, ormoni che a loro volta stimolano la sintesi di corticosteroidi. Poiché il cortisolo non può essere sintetizzato, questi ormoni vengono rilasciati in quantità elevate tanto da stimolare la produzione di altri steroidi surrenali. La forma più comune di iperplasia surrenale congenita è dovuta al deficit di steroide 21-monoossigenasi. Il 21-idrossilasi è necessario per la produzione sia di mineralcorticoidi che di glucocorticoidi, ma non di androgeni. Pertanto, la stimolazione ACTH della corticale surrenale induce il rilascio di quantità eccessive di androgeni surrenali, che possono portare allo sviluppo di genitali e caratteri sessuali secondari ambigui.[9]
Note modifica
- ^ Santulli G. MD, Adrenal Glands: From Pathophysiology to Clinical Evidence, Nova Science Publishers, New York, NY, 2015, ISBN 978-1-63483-570-1.
- ^ Adrenal gland, su Medline Plus/Merriam-Webster Dictionary. URL consultato l'11 febbraio 2015.
- ^ Ross M, Pawlina W, Histology: A Text and Atlas, 6th, Lippincott Williams & Wilkins, 2011, pp. 708, 780, ISBN 978-0-7817-7200-6.
- ^ a b c d e f g S Melmed, KS Polonsky, PR Larsen e HM Kronenberg, Williams Textbook of Endocrinology, 12th, Saunders, 2011, ISBN 978-1-4377-0324-5.
- ^ WL Miller e HS Bose, Early steps in steroidogenesis: intracellular cholesterol trafficking, in Journal of Lipid Research, vol. 52, n. 12, 2011, pp. 2111–2135, DOI:10.1194/jlr.R016675, PMC 3283258, PMID 21976778.
- ^ a b c d e D Longo, A Fauci, D Kasper, S Hauser, J Jameson e J Loscalzo, Harrison's Principles of Internal Medicine, 18th, New York, McGraw-Hill, 2012, ISBN 978-0-07-174889-6.
- ^ LK Nieman, Approach to the patient with an adrenal incidentaloma. [collegamento interrotto], in The Journal of Clinical Endocrinology and Metabolism, vol. 95, n. 9, 2010, pp. 4106–13, DOI:10.1210/jc.2010-0457, PMC 2936073, PMID 20823463.
- ^ Hydrocortisone Emergency Factsheet for Ambulance Personnel Archiviato il 24 settembre 2015 in Internet Archive. The Pituitary Foundation
- ^ E Charmandari, CG Brook e PC Hindmarsh, Classic congenital adrenal hyperplasia and puberty., in European Journal of Endocrinology, vol. 151, Suppl 3, 2004, pp. 77–82, DOI:10.1530/eje.0.151U077, PMID 15554890 (archiviato dall'url originale il 4 febbraio 2015).
Bibliografia modifica
- (EN) Adrenal Glands: From Pathophysiology to Clinical Evidence, New York, NY, Nova Science, 2015, ISBN 978-1-63483-570-1.
- Elaine N. Marieb, Il corpo umano: anatomia, fisiologia e salute, volume secondo, Zanichelli, 2004. ISBN 978-88-08-11259-0
- (EN) Santulli G. MD, Adrenal Glands: From Pathophysiology to Clinical Evidence, Nova Science Publishers, New York, NY, 2015, ISBN 978-1-63483-570-1.
- (EN) Ross M, Pawlina W, Histology: A Text and Atlas, 6th, Lippincott Williams & Wilkins, 2011, ISBN 978-0-7817-7200-6.
- (EN) S Melmed, KS Polonsky, PR Larsen e HM Kronenberg, Williams Textbook of Endocrinology, 12th, Saunders, 2011, ISBN 978-1-4377-0324-5.
- (EN) D Longo, A Fauci, D Kasper, S Hauser, J Jameson e J Loscalzo, Harrison's Principles of Internal Medicine, 18th, New York, McGraw-Hill, 2012, ISBN 978-0-07-174889-6.
Voci correlate modifica
Altri progetti modifica
- Wikizionario contiene il lemma di dizionario «surrene»
- Wikimedia Commons contiene immagini o altri file su surrene
Collegamenti esterni modifica
- surrene, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- (EN) Robert D. Utiger, adrenal gland, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Sezione al microscopio da www.bu.edu, su bu.edu.
- Sezione al microscopio da www.anatomyatlases.org, su anatomyatlases.org.
- Surrene, in Treccani.it – Enciclopedie on line, Roma, Istituto dell'Enciclopedia Italiana.
| Controllo di autorità | Thesaurus BNCF 11592 · LCCN (EN) sh85000998 · GND (DE) 4171381-3 · BNF (FR) cb119650578 (data) · J9U (EN, HE) 987007292945905171 · NDL (EN, JA) 00563655 |
|---|