Piombo tetraetile
Il Piombo tetraetile, conosciuto anche con la sigla TEL (dall'inglese tetraethyl lead), o PT.[2] È un composto metallorganico del piombo tetravalente, di formula molecolare Pb(CH2CH3)4. È molto tossico[3] ed è stato utilizzato in passato in petrolchimica come additivo per la benzina come antidetonante, per aumentarne cioè la resistenza all'auto-accensione (numero di ottano). È ancora di utilizzo comune in campo aeronautico per la produzione di benzina avio.
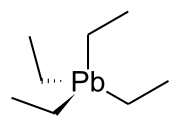
| Piombo tetraetile | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C8H20Pb |
| Massa molecolare (u) | 323,44 |
| Aspetto | liquido |
| Numero CAS | |
| Numero EINECS | 201-075-4 |
| PubChem | 6511 e 101498847 |
| SMILES | CC[Pb](CC)(CC)CC |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,653 |
| Temperatura di fusione | −136,8 °C (136,4 K) |
| Temperatura di ebollizione | 357 (84-85 °C a 15 mmHg) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 73 °C (346 K) |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 300 - 310 - 330 - 360 - 373 - 410 |
| Consigli P | 201 - 260 - 264 - 273 - 280 - 284 [1] |
Proprietà chimiche
modificaIl piombo tetraetile è un liquido viscoso incolore, dall'odore dolciastro e infiammabile. Si ottiene dalla reazione di cloruro di etile con una lega sodio-piombo:[4][5]
- 4 NaPb + 4 CH3CH2Cl → (CH3CH2)4Pb + 4 NaCl + 3 Pb
Dalla miscela di reazione il piombo tetraetile viene recuperato per distillazione in corrente di vapore, che non trascina la miscela residua di piombo metallico e cloruro di sodio.[6]
Il legame piombo-carbonio nel piombo tetraetile è debole, 130 kJ/mol, contro 346 kJ/mol per il legame C-C:[7] già a 110 °C inizia a decomporsi con un meccanismo a radicali liberi;[8] alle temperature raggiunte nei motori a scoppio si decompone quindi facilmente in piombo e radicali etile. In queste condizioni il piombo forma in parte l'ossido (PbO) solido; questo e il Pb metallico formato dalla decomposizione tenderebbero a incrostare le parti meccaniche. Per evitare questo inconveniente veniva utilizzato in miscela con 1,2-dicloroetano e 1,2-dibromoetano, con i quali forma composti volatili alle temperature raggiunte nei motori, quali il cloruro di piombo e il bromuro di piombo:[5][9]
- (CH3CH2)4Pb + C2H4Cl2 + 16 O2 → 10 CO2 + 12 H2O + PbCl2↑
- (CH3CH2)4Pb + C2H4Br2 + 16 O2 → 10 CO2 + 12 H2O + PbBr2↑
Le dosi massime sono dell'ordine di 0,5 g per litro di benzina, che corrispondono ad un aumento del numero di ottano di 10-15 unità. La ricetta tipica era del tipo:[5]
PbEt4 61,45%
C2H4Cl2 17,85%
C2H4Br2 18,80%
inerti e colore 1,90%
Storia
modificaIl possibile utilizzo del piombo tetraetile come antidetonante venne scoperto da Thomas Midgley alla General Motors Research nel 1921. La sua tossicità divenne evidente negli anni successivi con la malattia e talvolta la morte di alcuni dei ricercatori che si erano dedicati al suo studio. Il 1º febbraio 1923 cominciò la sua commercializzazione ad opera della Ethyl Gasoline Corporation, società compartecipata a DuPont, a General Motors e a Standard Oil. Già all'inizio della produzione gli operai addetti mostrarono segni di avvelenamento: almeno 15 morirono e per le restanti l'azienda disse che probabilmente erano impazzite "a causa del troppo lavoro"; nel 1924 cinque operai morirono ed altri 35 restarono invalidi, nonostante le prove le industrie commissionarono studi per smentire la pericolosità[10].
Anche in Italia (a Fidenza e a Trento) esistevano importanti industrie chimiche per la sua produzione. Clair Patterson scoprì che prima del 1923 i livelli di piombo nell'atmosfera erano insignificanti e si batté tutta la vita per denunciare il suo pericoloso utilizzo. A partire dagli anni settanta si susseguirono le iniziative per bandirlo dalla benzina, fino alla definitiva eliminazione nel 1986 negli Stati Uniti con il Clean Air Act e nel decennio successivo in Europa Occidentale[11]. Nel 1971 in ogni litro di benzina venduto in Germania erano presenti 0,635 grammi di piombo tetraetile[12] e la stessa concentrazione era in Italia il massimo ammesso[13].
In Italia il tenore massimo di piombo nella benzina fu ridotto nel 1982 a 0,40 grammi al litro, con possibilità di limitarlo fino a 0,15 grammi[14], possibilità sfruttata nel 1989, quando la concentrazione fu portata a 0,30 grammi, e ancora nel 1991, quando fu dimezzata[15]. Con l'eliminazione del piombo dai carburanti americani il livello del piombo nel sangue dei bambini fino a 5 anni, si è ridotto dell'80% e nei test di intelligenza effettuati su bambini in età prescolare si sono riscontrati medie tra 2,2 e 4,7 punti superiori al decennio precedente.
Citazioni letterarie
modificaÈ anche il veleno usato nel primo romanzo (giallo) di Ellery Queen, La poltrona n. 30.
Note
modifica- ^ Sigma Aldrich; rev. del 14.01.2012
- ^ SLOI. La fabbrica degli invisibili, a 3 min 26 s. URL consultato il 13 febbraio 2020.«...il piombo tetraetile, comunemente chiamato PT»
- ^ (EN) Karen I. Bolla e Jean Lud Cadet, Exogenous Acquired Metabolic Disorders of the Nervous System, Elsevier, 2007, pp. 865–896, DOI:10.1016/b978-141603618-0.10039-6, ISBN 978-1-4160-3618-0. URL consultato il 2 giugno 2022.
- ^ (EN) Dietmar Seyferth, The Rise and Fall of Tetraethyllead. 2., in Organometallics, vol. 22, n. 25, 1º dicembre 2003, pp. 5154–5178, DOI:10.1021/om030621b. URL consultato il 2 giugno 2022.
- ^ a b c Tetra-ethyl_lead, su chemeurope.com. URL consultato il 2 giugno 2022.
- ^ (EN) William E. Davis e United States Environmental Protection Agency Office of Air Quality Planning and Standards, Emission Study of Industrial Sources of Lead Air Pollutants, 1970, Environmental Protection Agency, 1973. URL consultato il 2 giugno 2022.
- ^ J. E. Huheey, E. A. Keiter e R. L. Keiter, Chimica Inorganica, Principi, Strutture, Reattività, Piccin, 1999, p. A-30, ISBN 88-299-1470-3.
- ^ F.A. Cotton e G. Wilkinson, ADVANCED INORGANIC CHEMISTRY, Fifth Edition, Wiley Interscience, 1988, pp. 293-294, ISBN 0-471-84997-9.
- ^ (EN) J. Theo Kloprogge, Concepcion P. Ponce e Tom Loomis, The Periodic Table: Nature's Building Blocks: An Introduction to the Naturally Occurring Elements, Their Origins and Their Uses, Elsevier, 18 novembre 2020, p. 826, ISBN 978-0-12-821538-8.
- ^ Bill Bryson. Breve storia di (quasi) tutto, Milano : Guanda, 2005, cap 10 Il piombo al bando
- ^ Bill Bryson. Breve storia di (quasi) tutto, Milano : Guanda, 2005, cap 10
- ^ c.g., Anche in Germania benzina senza piombo, in La Stampa, Torino, 1º maggio 1971, p. 19. URL consultato l'11 febbraio 2020.
- ^ Arturo Barone, Per le nuove norme sulla benzina Bonn è in contrasto con gli accordi Cee, in La Stampa, Torino, 21 marzo 1972, p. 12. URL consultato l'11 febbraio 2020.
- ^ Decreto del presidente della Repubblica 10 marzo 1982, n. 485, in materia di "Attuazione della direttiva (CEE) n. 78/611 relativa al contenuto di piombo nella benzina per i motori ad accensione comandata destinati alla propulsione degli autoveicoli"
- ^ Decreto ministeriale 28 maggio 1988, n. 214, in materia di "Attuazione della direttiva n. 85/210/CEE relativa al tenore di piombo nella benzina"
Bibliografia
modificaVoci correlate
modificaAltri progetti
modifica- Wikimedia Commons contiene immagini o altri file su piombo tetraetile
Collegamenti esterni
modifica- (EN) tetraethyl lead, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Scheda sulla sicurezza chimica per il piombo tetraetile, su cdc.gov. URL consultato il 7 gennaio 2006 (archiviato dall'url originale il 27 settembre 2005).
- Utilizzo del piombo tetraetile nei carburanti per MCI, su fuelcat.it. URL consultato il 7 gennaio 2006 (archiviato dall'url originale il 9 marzo 2005).
| Controllo di autorità | Thesaurus BNCF 22152 · LCCN (EN) sh87006520 · J9U (EN, HE) 987007534379005171 |
|---|