Peste
La peste è una malattia infettiva di origine batterica causata dal bacillo Yersinia pestis. È una zoonosi, il cui bacino è costituito da varie specie di roditori e il cui principale vettore è la pulce dei ratti (Xenopsylla cheopis) ma che può essere trasmessa da varie specie di parassiti ematofagi (come pulci, pidocchi, cimici dei letti) e che si può trasmettere anche da uomo a uomo. È una malattia quarantenaria e per il regolamento sanitario internazionale[1] è assoggettata a denuncia internazionale all'OMS, sia per i casi accertati sia per quelli sospetti. Dal 2010 al 2015 sono stati riportati 3 248 casi in tutto il mondo di cui 584 con esito mortale, ed è diffusa in tutti i continenti, fatta eccezione per Oceania ed Europa.[2]
| Peste | |
|---|---|
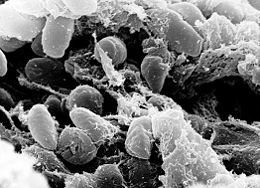 | |
| Specialità | infettivologia |
| Eziologia | Yersinia pestis |
| Classificazione e risorse esterne (EN) | |
| ICD-10 | A20 |
| MeSH | D010930 |
| MedlinePlus | 000596 |
| eMedicine | 235627 |
Si manifesta sotto forma di tre principali quadri clinici, distinti in base ai diversi apparati dell'organismo in cui si sviluppa l'infezione, detti peste bubbonica, setticemica e polmonare.
La peste bubbonica è causata dall'introduzione nell'organismo del bacillo Yersinia pestis attraverso la cute a seguito del morso di una pulce infetta; il bacillo, solitamente identificato dal sistema immunitario e fagocitato dai leucociti, viene smaltito attraverso il sistema linfatico fino ai linfonodi, dove però resta attivo e continua ad accumularsi moltiplicandosi. Ciò provoca una linfoadenopatia locale, cioè un'infiammazione di uno o più linfonodi, solitamente nella zona inguinale o ascellare più prossima alla zona della puntura. I linfonodi colpiti tendono a gonfiarsi, con sintomatologia dolorosa, e vengono detti appunto "bubboni"; questi non sono ascessi, bensì edemi: non contengono pus bensì sangue e tessuto edematoso-necrotico (possono però divenire superinfetti e quindi purulenti, anche in fase di remissione).
Quando i linfonodi non sono più in grado di contenere la malattia il bacillo può diffondersi in tutto l'organismo, dando luogo così alla seconda forma, la peste setticemica. Si tratta di un quadro clinico sistemico molto più grave: il bacillo, trasportato dal flusso sanguigno, raggiunge i principali organi dando luogo a una sepsi diffusa, condizione che, se non curata, può risultare fatale in breve tempo. Il terzo quadro clinico è la variante detta peste polmonare, estremamente grave, che si caratterizza per la diversa localizzazione in quanto si sviluppa nell'apparato respiratorio; a differenza della forma bubbonica, la peste polmonare è trasmessa per via aerea, viene contratta respirando particelle di saliva o altri liquidi provenienti da un individuo infetto ed è altamente contagiosa.[3]
I sintomi della malattia sono generici, comprendono febbre tra i 38 e i 41 °C, mal di testa, dolori articolari, nausea e vomito, sete, diarrea, tumefazione dei linfonodi e una generale sensazione di malessere. Nelle forme setticemiche e polmonari può verificarsi ipotensione, segni neurologici quali sonnolenza, letargia, delirio, e, nella forma polmonare, dispnea, tanto da conferire al malato un colorito cianotico. La sindrome da coagulazione intravascolare disseminata che può insorgere nella forma setticemica, e che è solitamente la causa del decesso,[4][5] ha come sintomo vistoso l'ischemia e necrosi delle estremità (dita, piedi o mani), che diventano nere; ciò ha probabilmente contribuito a coniare il nome peste nera per indicare la pandemia esplosa in Europa a metà del XIV secolo.
Se identificata tempestivamente, un pronto e corretto trattamento mediante la somministrazione di antibiotici può portare, nella maggioranza dei casi, a una prognosi positiva. La diagnosi può avvenire con certezza a seguito dell'identificazione del batterio in coltura da campioni biologici prelevati dal paziente; nella pratica non c'è il tempo di attendere un'indagine biologica, ci si affida a informazioni epidemiologiche sul contesto in cui si verifica l'infezione, e in presenza di sospetta diagnosi di peste si applica il protocollo terapeutico.[3]
Origine del nome modifica
Il termine pestilenza o peste (dal latino pestis, "distruzione, grande malattia") nell'Alto Medioevo, a causa delle limitate conoscenze scientifiche, era usato genericamente per indicare vari fenomeni epidemici caratterizzati da alta mortalità, come il colera, il morbillo o il vaiolo. Spesso ci si riferiva alla pandemia come febris pestilentialis, infirmitas pestifera, morbus pestiferus, morbus pestilentialis, mortalitas pestis o semplicemente pestilentia.[6]
La prima epidemia storicamente attribuibile con certezza a Yersinia pestis fu la peste di Giustiniano, che esplose a Costantinopoli verso la metà del VI secolo d.C. e si diffuse in Europa. Per quanto riguarda la pandemia del XIV secolo, l'espressione peste nera nacque dall'osservazione che nel Trecento si poté fare dei sintomi che essa provocava sulle persone, ovvero, fra gli altri, la comparsa di macchie scure e livide di origine emorragica che si manifestavano sulla cute e sulle mucose dei malati.[7]
Storia modifica
La peste ha avuto un impatto di straordinaria importanza nella storia umana. In particolare ha influenzato il corso della storia europea,[10] principalmente in due grandi pandemie: quella esplosa a Costantinopoli nella tarda antichità, a metà del VI sec. d. C. (peste di Giustiniano), che indebolì l'impero bizantino modificandone anche le capacità militari,[11] e quella che raggiunse l'Europa all'inizio dell'epoca moderna, alla metà del XIV secolo ("peste nera"), un evento di svolta epocale per i suoi effetti di riorganizzazione economica e demografica della società, ritenuto fondante del periodo definito epoca moderna.[12]
Probabile ruolo di altri patogeni in epidemie di epoca antica modifica
Anticamente il termine "peste" veniva utilizzato per indicare genericamente una "sventura", una "rovina", e pertanto vi sono molti riferimenti a casi di epidemia definiti morbus pestiferus, che potrebbero avere avuto come causa vari tipi di patogeno diversi da Y. pestis. Vi sono perciò talvolta dubbi se attribuire alcuni eventi epidemici del passato allo Yersinia pestis o ad altri agenti patogeni. Per esempio la celebre peste di Atene, raccontata da Tucidide e che colpì la città nel 430 a.C., secondo alcuni autori potrebbe essere stata il risultato di un'epidemia di vaiolo, mentre altri studiosi (Gomme et al., 1981) ritengono che fu una epidemia di tifo petecchiale.[13] Anche la peste antonina che colpì l'Impero Romano nel 167 d.C. durante il governo di Marco Aurelio si sospetta essere stata una epidemia di vaiolo. Altre probabilmente potrebbero essere state causate dalla varicella o dal morbillo.[14][15]
La peste di Giustiniano modifica
Si ritiene certo invece il coinvolgimento dello Y. pestis nella cosiddetta peste di Giustiniano che scoppiò nel 541 d.C. a Costantinopoli, la prima pandemia di peste documentata. Raccontata con dovizia di particolari dallo storico Procopio di Cesarea, che ne descrive le tipologie di sintomi e il decorso,[16] si ritiene che sia stata responsabile della morte di circa il 40% della popolazione della capitale bizantina per poi propagarsi, ricomparendo a ondate in modo localizzato, per tutta l'area mediterranea fino al 750 circa, causando un numero di vittime stimato tra i 50 e i 100 milioni. In virtù della sua estensione viene pertanto considerata la prima pandemia della storia.[17] Anche il mondo musulmano non fu risparmiato dalle ondate di questa pandemia: a partire dall'Egira si conoscono almeno cinque pestilenze: la peste di Shirawayh (627-628), la peste di 'Amwas (638-639), la peste violenta (688-689), la peste delle vergini (706) e la peste dei notabili (716-717).[18]
La peste nera modifica
La pandemia più celebre e devastante fu quella che dilagò intorno alla metà del XIV secolo nota come peste nera, considerata la seconda dopo quella di Giustiniano. Importata dal nord della Cina attraverso l'Impero mongolo, si diffuse in fasi successive alla Turchia asiatica ed europea per poi raggiungere la Grecia, l'Egitto e la penisola balcanica; nel 1347 si trasmise alla Sicilia e da lì a Genova; nel 1348 la peste nera aveva infettato la Svizzera tranne il cantone dei Grigioni e tutta la penisola italica tranne Milano; particolarmente violenta fu l'epidemia a Firenze, dove Giovanni Boccaccio ne fu testimone e compose il Decameron. Dalla Svizzera si allargò in Francia e in Spagna; nel 1349 raggiunse l'Inghilterra, la Scozia e l'Irlanda;[19] nel 1363, dopo aver infettato tutta l'Europa, i focolai della malattia si ridussero fino a scomparire.[20] Secondo alcuni studi uccise almeno un terzo della popolazione del continente,[21] portandola probabilmente da 45 milioni a 35–37,5 milioni.[22]
La pandemia durò oltre 300 anni continuando a ripresentarsi, anche se a ondate minori e via via più circoscritte, in molte città europee fino al 1720 circa. Al termine della prima ondata della grande pandemia, per la popolazione europea iniziò un periodo di continuo ripresentarsi della malattia con le conseguenti numerose vittime, seppur in misura minore rispetto alla prima ondata. È stato osservato che, tra il 1347 e il 1480, la peste colpì le maggiori città europee a intervalli di circa 6-12 anni affliggendo, in particolare, i giovani e le fasce più povere della popolazione. A partire dal 1480 la frequenza iniziò a diminuire, attestandosi a un'epidemia ogni 15-20 anni circa, ma con effetti sulla popolazione non certo minori.[23]
Le ondate successive modifica
Visto il continuo ripresentarsi dell'epidemia, le autorità cittadine europee adottarono misure per prevenirle o, perlomeno, per limitarne gli effetti. A Venezia nel 1423 venne realizzato un primo lazzaretto, mentre nel 1468 furono istituiti degli organismi permanenti di controllo, con la costituzione del Lazzaretto Nuovo[24]. A Milano fu istituito un ufficio di sanità permanente nel 1450 e realizzato il lazzaretto di San Gregorio nel 1488, progettato con la possibilità di espandere la propria capienza in caso di epidemia conclamata.[25] Per Firenze si dovette aspettare il 1527.[24] Parigi ne costituì uno nel 1580, ma già da circa 30 anni aveva affrontato il problema con l'emanazione di ordinanze e norme per affrontare le epidemie; a Troyes e a Reims gli uffici di sanità vennero creati, rispettivamente, nel 1517 e nel 1522.[26] Verso la fine del XVI secolo Amsterdam istituì un servizio di rimozione dei rifiuti dalle strade al fine di migliorare le condizioni igieniche nel tentativo di prevenire focolai epidemici, costruì un lazzaretto e decise di porre un medico professionista tra i magistrati che si occupavano della sanità pubblica.[26] A Londra si preferì ancora, in caso di epidemia, la segregazione domiciliare piuttosto del confinamento in un lazzaretto.[27]
Il XVI secolo e la fine delle epidemie europee modifica
Nonostante l'adozione di tutti questi accorgimenti, la peste continuò a ripresentarsi e a mietere vittime. Notevoli epidemie si registrarono nel territorio milanese nel biennio 1576-1577, a San Cristóbal de La Laguna del 1582, nell'Italia settentrionale nel 1630 (raccontata anche da Alessandro Manzoni nei Promessi Sposi) e a Siviglia tra il 1647 e il 1652. Nel 1661 l'Impero ottomano fu pesantemente colpito mentre, tra il 1663 e il 1664 un'epidemia si propagò nella repubblica olandese uccidendo 35 000 persone nella sola Amsterdam.[28] La grande peste di Londra colpì la capitale britannica tra il 1665 e il 1666, causando la morte di un numero di persone compreso tra i 75 000 e 100 000, vale a dire più di un quinto dell'intera popolazione della città.[29] L'ultima grande epidemia, e una delle più devastanti che abbia afflitto una grande città, fu quella che interessò Marsiglia nel 1720 arrivando a uccidere quasi il 50% di tutta la popolazione cittadina, a cui si dovettero aggiungere le vittime residenti nelle zone limitrofe.[30]
La terza pandemia modifica
Una terza pandemia ebbe inizio intorno al 1855 nella provincia cinese di Yunnan per poi diffondersi globalmente verso la fine del secolo.[31] Si stima che tra il 1898 e il 1918 morirono di peste circa 12,5 milioni di indiani.[32] Nel 1894, in occasione della manifestazione dell'epidemia a Hong Kong il batteriologo franco-svizzero Alexandre Yersin riuscì a scoprire e isolare il batterio responsabile della malattia, successivamente chiamato Yersinia pestis.[33][34] Nel 1898 Paul-Louis Simond spiegò che tale bacillo si poteva trasmettere attraverso il morso di pulci che si erano infettate dai roditori.[33] Per il resto del XX secolo i focolai della malattia continuarono ma con tassi di mortalità di molto inferiori alle precedenti epidemie, grazie all'introduzione di efficaci misure di sanità pubblica e, a partire dagli anni cinquanta del Novecento, degli antibiotici. Tuttavia, la peste è rimasta come malattia enzootica dei roditori in quasi tutto il mondo con l'esclusione dell'Australia.[32]
Epidemiologia modifica
La peste viene talvolta, erroneamente, considerata una malattia del passato, poiché negli ultimi secoli non vi sono più state grandi epidemie, e le ondate epidemiche catastrofiche che hanno raggiunto le dimensioni di pandemia, causando decine di milioni di morti, si sono sviluppate nel medioevo o nella tarda antichità.[35] Tuttavia, il batterio non è stato debellato. Non può essere eradicato essendo presente in ampi bacini di popolazioni di molte specie animali, e rimane una minaccia latente con cui molte popolazioni umane devono fare i conti, in particolare alcune popolazioni residenti in Africa. A partire dagli anni novanta del Novecento si è registrato un aumento dei casi annui, facendo sì che la peste venisse classificata come una malattia riemergente.[36][37] Vi sono alcuni fattori per cui le popolazioni del continente africano sono maggiormente a rischio: i gruppi di persone più povere vivono tuttora a contatto ravvicinato con colonie di roditori, che talvolta vengono cacciati e mangiati; inoltre, superstizioni locali e carenza di servizi sanitari possono ostacolare la profilassi, e comportare ritardi nel trattamento e nel contenimento del focolaio. I territori contenenti habitat naturali di praterie o savana sono più portati all'endemismo.[37]
A partire dalla fine del XX secolo, a livello globale, ogni anno vengono segnalati circa 600 casi di peste, distribuiti su ampie zone che comprendono l'Asia, l'Eurasia, l'Africa e le Americhe.[3][35][38] Dal 2001 al 2018 l'Organizzazione Mondiale della Sanità (OMS) ha segnalato il verificarsi di almeno 14 focolai giudicati di rilievo. Nel 2017 i Paesi con il maggior numero di persone infette erano la Repubblica Democratica del Congo, il Madagascar e il Perù.[35]
Nel decennio che va dal 1998 al 2008, sono stati registrati dall'OMS almeno dai 1 000 ai 5 000 casi di peste riguardanti l'uomo, che hanno causato dai 100 ai 200 decessi; tuttavia si stima che per via della carenza di strutture dedicate alla diagnosi nei paesi colpiti, tali numeri possano essere ben più elevati. La maggior parte di essi ha riguardato la peste nella sua forma "bubbonica", trasmessa agli uomini dai ratti attraverso le pulci; tuttavia si rilevano anche alcuni, seppur sporadici, casi di forma "polmonare".[37]
Nonostante quasi tutti i casi si verifichino in zone endemiche, la possibilità di viaggiare in tempi brevi su larghe distanze non esclude che vi possano essere manifestazioni della malattia in qualsiasi altra zona del mondo; è stato, ad esempio, il caso di un focolaio riscontrato nel dicembre 2014 tra alcuni minatori della Repubblica Democratica del Congo probabilmente importato da qualcuno proveniente da una zona endemica, arrivando fino alla città di Kisangani.[37][39] Infine, la prevalenza della peste è maggiore nei paesi con climi caldi e tra le popolazioni più povere. Il 50% dei casi riguarda persone di età compresa tra i 12 e i 45 anni; il sesso maschile appare più colpito rispetto alle donne e vi è un'incidenza maggiore tra coloro che svolgono attività all'aperto.[40]
Eziologia modifica
L'agente eziologico di tutte le manifestazioni cliniche della peste è il bacillo Yersinia pestis. Si tratta di un coccobacillo Gram-negativo, immobile e psicrofilo. È lungo circa 1-3 μm e largo 0,5-0,8 μm. Fa parte del gruppo dei batteri detti "non coliformi", cioè che non sono in grado di fermentare il lattosio. Come gli altri bacilli ha una catalasi positiva, ovvero è in grado di dissociare l'acqua ossigenata (H2O2) in acqua e ossigeno. La sua fermentazione è acido-mista e si sviluppa meglio in terreni di coltura contenenti sangue.[3][32] Si sviluppa a temperature comprese tra i 4 e i 40,8 °C (optimum tra i 28 e i 30,8 °C) con pH ottimale tra 7,2 e 7,6; è in grado comunque di tollerare un range di pH compreso tra 5 e 9,6.[32] In coltura e alla colorazione di Giemsa, di Wright o di Wayson presenta un caratteristico cromatismo bipolare, con le estremità colorate intensamente e con bordi ad arco, una forma che ricorda vagamente una spilla da balia.[32]
Lo Y. pestis deve il suo nome allo scienziato Alexandre Yersin, che lo isolò per la prima volta in occasione dell'epidemia scoppiata a Hong Kong nel diciannovesimo secolo.[3][41]
Il genere Yersinia, cui il batterio appartiene, è a sua volta appartenente alla famiglia degli Enterobacteriaceae, composta da undici specie (circa venti secondo autori recenti), tre delle quali sono patogene per gli umani, strettamente imparentate fra loro: oltre allo Y. pestis, lo Y. pseudotuberculosis e lo Y. enterocolitica; questi ultimi due causano enterocoliti, di entità solitamente lieve.[3][5][40][41]
La specie umana non è un ospite ideale per Y. pestis, che solo occasionalmente ha causato epidemie umane in particolari condizioni igienico-sanitarie e climatiche; la presenza del batterio è invece endemica e permanente in molte specie di mammiferi, tra cui sembra prediligere quali foci i roditori; è anche patogeno per alcune specie di uccelli.[32] I mammiferi ospiti frequenti sono molti, tra cui conigli e pipistrelli, ma anche cani e gatti occasionalmente possono contrarre l'infezione. Il ciclo di trasmissione di Y. pestis è strettamente legato alle pulci, e sono queste i veri agenti di contagio. I roditori sono gli ospiti principali dello Y. pestis, e in ambiente naturale questi sono rappresentati da specie selvatiche; in ambienti urbani o antropizzati, invece, le specie ospiti principali sono il Rattus rattus e il Rattus norvegicus, i quali possono condividere gli spazi con l'uomo o entrare in contatto con animali domestici. Non sempre i ratti infetti manifestano sintomi gravi, e talvolta possono essere portatori asintomatici. Il vettore principale con cui si trasmette, sia agli animali sia all'uomo, sono le pulci, in particolare la Xenopsylla cheopis (la pulce di ratto orientale), ma anche la Pulex irritans.[40]
Lo Y. pestis è un patogeno relativamente "giovane"; si ritiene che sia una variante, sviluppatasi come clone genetico circa 5 000-7 000 anni fa, dello Yersinia pseudotuberculosis in seguito all'acquisizione da parte di quest'ultimo di tre plasmidi patogeni (pMT1, pPCP1 e pCD1) che gli hanno permesso di implementare un ciclo vitale trasmissibile attraverso le pulci e la capacità di causare un'infezione sistemica dell'ospite. Durante la sua evoluzione, lo Y. pestis ha dimostrato un tasso di mutazione variabile non sempre conforme all'orologio molecolare.[3][40][42][43]
Trasmissione modifica
Il ciclo di trasmissione di Y. pestis è ben conosciuto. Studi approfonditi furono compiuti alla fine del diciannovesimo secolo in corrispondenza della terza pandemia, quando si erano osservate invasioni di ratti, i quali apparivano colpiti dal contagio, nei centri urbani delle aree asiatiche nei momenti appena precedenti o in concomitanza dei picchi epidemici. Nel 1898 l’infettivologo Paul-Louis Simond fu in grado di provare che la malattia si trasmetteva dai roditori, commensali all’uomo, agli umani, non direttamente bensì attraverso le pulci che potevano parassitare entrambe le specie.
Subito dopo la scoperta di Simond, il meccanismo di interazione del batterio con la pulce ospite-vettore fu studiato con dovizia di dettagli dall’entomologo Arthur William Bacot, che lo descrisse la prima volta in relazione alla pulce dei ratti orientale (Xenopsylla cheopis). Bacot osservò le fasi della colonizzazione da parte di Y. pestis della superficie interna del tratto digerente dell’insetto, e i meccanismi fisiologici prodotti dal batterio sulla pulce che stanno alla base della meccanica della sua trasmissione ai mammiferi e all’uomo.
L’acquisizione del batterio da parte della pulce vettore avviene quando questa si alimenta del sangue di un animale portatore di infezione. La pulce viene infettata a sua volta dal batterio, il quale colonizza l’esofago dell’insetto formando un biofilm che arriva ad ostruire il proventricolo (una parte del sistema digerente che negli insetti ha funzione masticatoria) e impedisce quindi alla pulce la deglutizione del sangue ingerito.[44][45] Mentre si alimenta del sangue dell'ospite la pulce tenta di deglutire il sangue ingerito, ma a causa dell’ostruzione dell’esofago lo rigurgita nuovamente all’interno del corpo dell’ospite, insieme a frammenti che si staccano dal coagulo batterico (o biofilm). La pulce spinta dalla fame compie tentativi ripetuti di alimentarsi e può pungere altri ospiti prima di morire.[33][37][46]
Gli ospiti più comuni per il batterio della peste sono i roditori, tanto che si ritiene che il bacillo possa trovarsi nell’ambiente in forma endemica praticamente solo nelle loro tane. L’ospite preferenziale originario del vettore X. cheopis è il rattus norvegicus (ratto delle chiaviche), una specie il cui areale di origine è probabilmente la Manciuria (Cina nord-orientale) ma che è divenuta cosmopolita e commensale dell’uomo e una delle specie più invasive oggi diffusa in tutto il mondo.
In seguito alle scoperte di Simond e Bacot si è ritenuto a lungo che la pulce dei ratti fosse il vettore unico di Y. pestis. Sulla scorta di tale assunto si riteneva che la malattia umana fosse causata necessariamente da una convivenza tra specie umana, roditori e pulci. Tuttavia lo stesso Bacot, in lavori appena successivi, osservò che Y. pestis è in grado di compiere l’identico ciclo di trasmissione utilizzando come vettori anche altre specie di insetti parassiti, ad esempio le cimici dei letti (Bacot 1915).[47] Anche la pulce del gatto, la pulce del cane e la pulce umana (pulex irritans) hanno la stessa potenzialità di infettarsi e di fungere da vettori per il bacillo.[37][48]
Del resto l’invasione delle città da parte di ratti infetti, fenomeno vistoso durante la terza pandemia, non era stata osservata in altre epidemie del passato: le fonti medievali sulla Peste Nera non riportano il fenomeno del contagio fra i ratti, un aspetto che era invece risultato caratteristico nell’epidemia moderna, specialmente in India. Gli studi recenti hanno rivisto i modelli epidemiologici della Peste Nera giungendo alla conclusione che la pandemia del quattordicesimo secolo in area Europea secolo fosse trasmessa direttamente da uomo a uomo, senza la mediazione di roditori, e per lo più da vettori parassiti esclusivamente umani.[49] I modelli considerati hanno fatto ipotizzare che il vettore di trasmissione più probabile fosse il pidocchio del corpo, un parassita umano che vive negli indumenti tessuti con fibre animali come la lana, cioè il tipo di indumenti utilizzati in Europa in quell'epoca e che non potevano essere lavati frequentemente.[50] Una ricerca recente sulla dinamica dell'epidemia medievale nel villaggio britannico di Eyam, ha concluso che circa il 90% dei contagi sarebbe avvenuta direttamente da uomo a uomo, in maggioranza tra familiari.[51] Un ulteriore studio di statistica epidemica (ottobre 2022) ha dato risultati in accordo con i precedenti studi, concludendo che molto probabilmente nessuna specie animale ha costituito una riserva del batterio in Europa durante le epidemie storiche, in nessun periodo, mentre le dinamiche di diffusione indicherebbero un meccanismo di contagio tramite parassiti esclusivamente umani.[52][53]
Ciclo di trasmissione e tossicità di Y. pestis modifica
La capacità di Y. pestis di sopravvivere all’interno del sistema digerente degli insetti parassiti, che lo differenzia dalle altre specie del genere yersinia, potrebbe essere all’origine della sua pericolosità per gli esseri umani. La tossicità del batterio Y. pestis per molti organismi animali, ovvero ciò che causa la gravità dei sintomi, lo differenzia dalle altre venti specie circa della stessa famiglia (come ad esempio Y. pseudotubercolosis) che nonostante la loro forte somiglianza con il bacillo della peste, sono scarsamente patogene o innocue per l’uomo. La specie Y. pestis è l’unica in grado di resistere all’interno del tratto digerente degli insetti, tale caratteristica evolutiva è correlata a una variante proteica presente sulla superficie del batterio, una proteina detta tossina murinica yersinica.
Recenti studi hanno concluso che la sopravvivenza di Y. pestis nell’apparato digerente dell’insetto è favorita da alcune proteine prodotte dal batterio, tra cui la tossina murina yersinica (Yersinia murine toxin - Ymt) che però è molto tossica per i roditori e ne causa i sintomi.[54]
I livelli in cui Y. pestis esprime la sua virulenza negli organismi animali sono almeno due. Ad un primo livello, tale virulenza è dovuta a sistemi di tipo chimico e fisico mediante i quali il batterio inibisce il sistema immunitario dell’ospite, in particolare riuscendo a bloccare la fagocitosi da parte dei macrofagi e diventando un parassita intracellulare. Ciò causa un rallentamento della risposta immunitaria dell’ospite, consentendo la replicazione del batterio. Il batterio Y. pestis è un parassita intracellulare facoltativo: può cioè entrare all’interno delle cellule dell’ospite e lì sopravvivere.
Quando è all’interno della cellula ospite il batterio non è in grado di esprimere tutte le funzioni ma è comunque in grado di produrre alcuni antigeni, detti W e V, che inibiscono la sua uccisione mediante fagocitosi intracellulare, perciò consentendo la sopravvivenza di una certa quota di batteri. I batteri che sopravvivono all’interno dei macrofagi vengono trasportati fino ai linfonodi, dove si accumulano.
Nella fase di proliferazione extracellulare, i batteri esprimono più funzioni e producono antigeni, detti F1, i quali possono essere identificati dai neutrofili, rendendo possibile per il sistema immunitario individuare il patogeno. Il sistema immunitario sviluppa così una risposta antigene-specifica ed è in grado di eliminare progressivamente il batterio. L’organismo deve però avere il tempo per produrre sufficienti neutrofili istruiti contro gli antigeni.
Questa capacità anti-fagocitosi di Y. pestis conferisce al batterio una certa capacità di sopravvivenza nell’organismo dell'ospite, poiché causa il rallentamento della risposta immunitaria; ma la grave tossicità per il sistema sembra essere causata dalle proteine che proteggono il batterio presenti sulla sua membrana esterna, specialmente la tossina murina yersinica la cui funzione è quella di protegge il bacillo dagli enzimi presenti nel tratto digerente degli insetti vettori. Questa tossina scatena shock sistemici in molte specie animali. La tossicità di Y. pestis per i mammiferi sembra quindi collegata evolutivamente al suo ciclo di trasmissione attraverso gli insetti.
Trasmissione nei roditori e altri mammiferi modifica
Gli insetti parassiti sono il vettore di trasmissione principale fra gli animali non umani. Tra i roditori, diverse specie mostrano una resistenza alla malattia variabile da individuo a individuo. La caratteristica degli individui resistenti potrebbe essere adattiva. È stato osservato che una quota di individui di Rattus norvegicus restano asintomatici o paucisintomatici, pertanto sono ospiti adatti a diffondere il contagio. I gatti possono infettarsi tramite il contatto con i roditori o con le loro pulci, specie in aree di endemismo - come le praterie - dove i felini domestici sono un possibile veicolo di contagio per l’uomo. I gatti in genere non sopravvivono all’infezione, mentre i cani di solito sopravvivono e costituiscono una barriera alla diffusione del contagio. Gli esseri umani possono infettarsi tramite la manipolazione di tutti gli animali infetti, o della loro carne.
Trasmissione della forma polmonare modifica
Oltre ai meccanismi correlati a vettori e ospiti animali, è possibile la trasmissione diretta tra individui della forma polmonare, che avviene attraverso le esalazioni respiratorie. Alcuni dei picchi epidemici della terza pandemia di peste sono stati di peste polmonare. In particolare vi fu una epidemia di peste polmonare in Manciuria, che esplose nella città di Harbin e si estese ad altre città in Cina e in Mongolia dall’autunno del 1910 alla fine del 1911, causando circa 60.000 vittime.[55][56] Al momento della ricomparsa di nuovi focolai negli anni ‘20 del ventesimo secolo, nelle città cinesi si ebbe un numero di vittime di poche migliaia, per effetto di disposizioni sanitarie più efficaci da parte delle autorità.
In diverse epoche in alcune aree del mondo vi sono state epidemie di peste polmonare, ma questa forma si è presentata con focolai geograficamente circoscritti e in generale non ha caratterizzato le epidemie nell’area europea. Nella parte introduttiva del Decameron, Giovanni Boccaccio riferisce che all’arrivo della peste a Firenze nel 1348, la pandemia era ormai attesa, poiché era noto che il contagio era presente nell’Asia Orientale da alcuni anni e si stava avvicinando; tuttavia, riferisce che la peste si manifesta in Europa in una forma, quella bubbonica, che era diversa da quella apparsa in oriente: nell’epidemia europea erano assenti i sintomi respiratori, come l’emottisi, che avevano colpito le persone in oriente ed erano tali che “a chiunque uscisse sangue dal naso, era destinato a morire”; comparivano invece i bubboni e l'infezione non era sempre mortale.[57]
La peste polmonare è altamente contagiosa e la trasmissione avviene in genere direttamente da persona a persona con le modalità caratteristiche delle infezioni respiratorie, principalmente attraverso la tosse. Anche i gatti possono sviluppare la malattia polmonare e quindi trasmetterla agli uomini con le stesse modalità.[40][58] Questa forma, che se non curata tempestivamente è quasi sempre letale, ha un decorso estremamente rapido ed è tipicamente bifasica: la prima fase è caratterizzata da sintomi febbrili e di affezione polmonare generica ed è seguita da una fase di deterioramento di grande rapidità con un andamento specifico.[59] La brevità del decorso e l’estrema letalità della malattia sono fattori intrinseci che fungono da argine alla diffusione di questa forma, e hanno contribuito a consentire la limitazione dei focolai.
Clinica modifica
La peste si manifesta principalmente nella forma di tre diversi quadri clinici: la peste bubbonica, la peste polmonare e la peste setticemica.[60] I quadri si differenziano sulla base degli apparati diversi dell'organismo in cui si sviluppa l'infezione. Le due ultime forme possono manifestarsi come quadri a sé stanti, oppure, più frequentemente, come complicazione o evoluzione della prima forma. L'accertamento della peste bubbonica si può determinare analizzando l'interno dei bubboni per la presenza di Yersinia pestis, mentre è possibile rilevare quella setticemica attraverso un'emocoltura.[40]
Peste bubbonica modifica
La peste bubbonica è un'infezione batterica che si sviluppa e si concentra prevalentemente nel sistema linfatico. La trasmissione nell'uomo può avvenire attraverso la puntura delle pulci dei ratti (come la Xenopsylla cheopis), o tramite il morso dei ratti stessi o di altri roditori infetti, inoculando così attraverso la cute il bacillo Y. pestis. La pulce dell'uomo, i pidocchi e le cimici dei letti hanno, virtualmente, la capacità di trasmettere la peste bubbonica anche da uomo a uomo. Una volta entrato nell'organismo, il bacillo si diffonde nei linfonodi più vicini, solitamente quelli ascellari o inguinali.[61][62]
Insorge violentemente dopo un periodo di incubazione da due a dodici giorni. Si presenta con febbre alta, cefalea, grave debolezza, disturbi del sonno, nausea, fotosensibilità, dolore alle estremità, vomito, dolore addominale. Tra i primi segni si può formare una pustola o necrosi che interessa la superficie cutanea nell'area della puntura dalla pulce infetta. A causa dell'incubazione piuttosto lunga i pazienti di solito non ricordano la puntura dell'insetto o il momento del contatto con animali. È possibile talvolta la formazione di petecchie, diffuse su una porzione vasta di superficie corporea, generalmente in modo asimmetrico o irregolare. Le manifestazioni cutanee non sono sempre presenti né specifiche.
L'aspetto clinico più caratteristico della malattia è l'ingrossamento di uno o più linfonodi, prossimi al luogo delle punture della pulce (che è più frequentemente la zona inguinale e quella ascellare). Il linfonodo infiammato viene denominato bubbone, ovvero un rigonfiamento edematoso il cui interno evolve formando un accumulo emorragico e necrotico. Ciò è la conseguenza del fatto che il batterio Y. pestis continua a sopravvivere anche dopo essere stato fagocitato dai leucociti e si accumula all'interno del linfonodo, riproducendosi e producendo tossine beta-bloccanti e in grado di bloccare alcune risposte immunitarie.[63]
La maggioranza dei pazienti presenta un solo bubbone. Il 70% dei pazienti presenta un linfonodo ingrossato in area inguinale, nei restanti casi la sede è il collo o la nuca, o la catena di linfonodi ascellari, o la regione femorale. I bubboni generalmente non sono appariscenti: possono avere qualsiasi dimensione compresa tra 1 e 10 centimetri, la loro localizzazione è profonda, sono soffici al tatto e dolorosi. Spesso sono visibili solo con una indagine ecografica, o una piccola area di cute eritematosa può essere unico indizio della loro presenza. Se i bubboni sono duri e tesi è indizio che sono superinfetti, e in alcuni casi si possono trattare come ascessi, applicando però rigorose misure di protezione. È anche possibile la formazione di bubboni nella regione mesenterica, causando dolore addominale.
La forma bubbonica, se non curata, nel 40% dei pazienti evolve in una forma più grave. Quando ciò avviene l'infezione si propaga nell'organismo, dando luogo alla peste setticemica descritta sotto, provocando insufficienza cardiocircolatoria, necrosi che solitamente partono dalle dita di mani o piedi per poi espandersi lentamente, complicazioni renali o emorragie interne. In assenza di cure, la malattia può evolvere verso questa fase e portare facilmente alla morte. In alcuni casi (intorno al 5%) si ha meningite, di solito preceduta da batteriemia, e può esservi coinvolgimento dell'encefalo, con sintomi gravi tra cui delirio. Un'altra evoluzione possibile del quadro infettivo è la peste polmonare, anch'essa descritta sotto. Alternativamente, nei casi meno gravi, la febbre cessa dopo circa due settimane. In taluni casi si hanno postumi tra i quali il drenaggio spontaneo di bubboni superinfetti, che espellono pus e formano una cicatrice.[61][62]
Peste setticemica modifica
È la setticemia sistemica derivante dalla propagazione di Y. pestis nell'apparato circolatorio che lo porta a raggiungere tutte le parti dell'organismo. Può seguire come seconda fase in conseguenza del cedimento di uno o più linfonodi quando questi, già trasformati in bubbone in un processo di infiammazione emorragica, non sono più in grado di contenere il batterio al loro interno. In questo quadro le tossine batteriche che circolano liberamente possono determinare sindromi da coagulazione intravascolare disseminata (CID) che colpiscono a partire dalle estremità, causando necrosi di dita o piedi, ecchimosi diffuse sull'intera superficie del corpo, e vengono esaurite le capacità coagulatorie del corpo causando emorragie negli organi interni. La CID costituisce un quadro estremamente pericoloso che deve essere trattato in modo aggressivo e tempestivamente, in caso contrario conduce alla morte nel corso di poche ore. Il quadro setticemico produce facilmente scompensi renali, cardiocircolatori e sindromi multi-organo.[4][61][62]
L'insorgenza di questa forma è solitamente mortale in un tempo molto breve, dell'ordine di un solo giorno, se non curata. Il trattamento con antibiotici riduce drasticamente la mortalità, a condizione che sia molto tempestivo.[3]
Peste polmonare modifica
Forma decisamente più grave rispetto alla peste bubbonica, è caratterizzata dalla localizzazione nell'apparato respiratorio, in quanto un focolaio di infezione si sviluppa nei polmoni. Può presentarsi anche come complicanza della forma bubbonica, ma più spesso è indicatore della diversa modalità con cui si è contratto il batterio (non attraverso la puntura della pulce ma respirando materiale infetto). Il periodo di incubazione è in genere più breve, da uno a sette giorni, e il quadro si presenta come una polmonite dal decorso fulminante, che all'esame radiografico mostra un infiltrato scarso rispetto alla gravità del quadro. Il primo sintomo può essere febbre alta, superiore a 39 °C, seguita da un deterioramento molto rapido delle condizioni generali. In un periodo di tempo breve, che può essere dell'ordine di 1-2 giorni, si ha una progressione verso una fase terminale che può comportare anche un notevole abbassamento della temperatura corporea, oltre che dispnea (difficoltà respiratorie), tosse, emottisi, cianosi (colorazione bluastra della pelle e delle mucose, sintomo di disturbi circolatori o respiratori) e grave debolezza. È caratterizzante di questa forma anche la batteriemia e l'insorgenza di gravi disturbi neurologici. Se non viene curata in tempo, porta quasi sicuramente alla morte per edema polmonare acuto.[61][62][64] Se non trattata tempestivamente la forma polmonare risulta fatale nella quasi totalità dei casi.[65]
La peste polmonare è trasmissibile anche senza l'azione di pulci, per via aerea: attraverso, cioè, tosse e starnuti di persone infette, contenenti materiale infetto in aerosol che potrebbe contagiare un prossimo ospite.[61][62][64]
Altre forme di peste modifica
Yersinia pseudotuberculosis è un batterio appartenente allo stesso genere Yersinia che dà luogo a un quadro subacuto o cronicizzante con sintomi prevalentemente gastroenterologici. L'infezione si localizza in linfonodi profondi in area addominale causando adenite mesenterica, condizione che potrebbe indurre a sospettare tubercolosi (da cui il nome del batterio). È una infezione rara negli esseri umani.[66][67]
Yersinia enterocolitica è anch'esso un batterio appartenente allo stesso genere che colpisce principalmente il basso tratto digerente, ma è molto più frequente nell'uomo. Esso dà luogo a sintomi gastroenterologici più chiaramente conclamati rispetto a Y. pseudotuberculosis.[68]
Diagnosi modifica
Una corretta e rapida diagnosi è fondamentale per il successo del trattamento del paziente e per limitare il diffondersi di un'epidemia. Secondo quanto dettato dalle linee guida dell'Organizzazione Mondiale della Sanità, la peste può essere diagnosticata come un caso sospetto, presunto o confermato sulla base di elementi sia clinici sia di laboratorio.[3] In ogni caso, è indicato che qualsiasi individuo che dovesse essere ritenuto contagiato dal batterio sia messo in isolamento per via della possibile alta contagiosità. I centri per la prevenzione e il controllo delle malattie (CDC) statunitensi prevedono, per il personale di assistenza nei casi di peste polmonare, l'utilizzo di precauzioni standard.
Inoltre, è ritenuto necessario che anche il personale di laboratorio che esegue i test sui campioni biologici del possibile infetto, sia informato del sospetto affinché adotti le corrette misure cautelative.[40]
Il gruppo di ricerca franco-malgascio guidato da Suzanne Chanteau dell'Istituto Pasteur del Madagascar (IPM) ha sviluppato nel 2003 un test rapido per la diagnosi di peste polmonare e bubbonica, che consente il rilevamento degli anticorpi entro quindici minuti.[69] Con 4 000 casi di peste che si verificano annualmente in tutto il mondo, una diagnosi rapida entro 24 ore è una componente cruciale per il successo del trattamento. In venti Paesi, soprattutto in Africa, la peste è ancora in atto.[70]
Diagnosi clinica modifica
La genericità dei sintomi costituisce la maggiore problematica nella diagnostica iniziale di questa patologia, che peraltro è anche caratterizzata spesso da rapida evoluzione. A causa della genericità dei sintomi, la certezza della diagnosi di regola è impossibile su basi puramente cliniche, ma è possibile identificare un caso sospetto o presunto. Per una diagnosi probabile, oltre prendere in considerazione i dati clinici cioè i segni e i sintomi tipici della malattia valutabili attraverso una visita medica correlata da anamnesi, è necessario valutare il contesto epidemiologico che accompagna il paziente, vale a dire la sua residenza o provenienza da una zona endemica entro circa dieci giorni dalla prima manifestazione della condizione, o la sua possibile esposizione a pazienti affetti o animali infetti e/o una evidente storia di punture di pulci.[3][71] Quando sussistono tutte queste condizioni è possibile diagnosticare un caso presuntivo di peste, che andrà, ove ve ne è la possibilità, confermato attraverso analisi di laboratorio.[3]
Diagnosi di laboratorio modifica
Quando si è diagnosticato un caso di peste presunta, è necessario procedere a esami di laboratorio il cui gold standard per la conferma rappresenta l'isolamento e l'identificazione dello Yersina pestis nei campioni biologici prelevati dal paziente come dal sangue o dal fluido aspirato dai bubboni. Tale patogeno si sviluppa su diversi terreni di cultura, come l'agar MacConkey, l'agar cuore-cervello e l'agar sangue, a una temperatura ottimale tra i 26 e i 28 °C, ma è necessaria una temperatura di 37 °C di incubazione perché si produca l'antigene F1. Dopo circa 24 ore dall'incubazione, il bacillo Y. pestis è visibile alle varie colorazioni di Giemsa, di Wright o di Wayson. L'isolamento del bacillo deve essere eseguito in un laboratorio con livello di biosicurezza minimo di classe 3.[3]
L'antigene F1 viene in genere utilizzato come bersaglio per rilevare lo Y. pestis con metodi immunologici. Un test di inibizione dell'emoagglutinazione dell'antigene F1 viene convenzionalmente impiegato per rilevare l'antigene F1 nel campione biologico.[72] Sono stati riportati anche test di immunofluorescenza e test immunoenzimatico per rilevare quantitativamente l'anticorpo F1 o l'antigene F1.[73] Lo Y. pestis può essere rilevato anche mediante reazione a catena della polimerasi (PCR) mirando al gene dell'antigene F1 (caf1), al gene pla o ai frammenti cromosomici (come il frammento 3a).[58][74] Tuttavia, è stato dimostrato che i bersagli del gene pla e del frammento cromosomico non sono affidabili per rilevare il batterio. La rilevazione immunologica, basata sull'acido nucleico dello Y. pestis può essere eseguita in un laboratorio di livello 2 di biosicurezza.[3]
Nelle zone endemiche della malattia e in cui non vi è la disponibilità di un laboratorio in grado di eseguire l'isolamento del batterio o l'identificazione immunologica o molecolare del batterio, è possibile procedere con altri test come il test rapido immunocromatografico in grado di confermare l'esistenza dell'antigene F1 da campioni clinici. Per ottenere risultati affidabili è però necessario che tale esame sia svolto da personale ben addestrato.[69] Anche il ricorso a termociclatori portatili può essere utile per rilevare il patogeno della peste direttamente sul posto.[3][75]
Diagnosi differenziale modifica
Per ogni presentazione clinica della peste (bubbonica, setticemica, polmonare) vi è un'ampia possibilità di diagnosi differenziale. Nel caso di peste bubbonica è necessario escludere altre cause di linfoadenopatia (ingrossamento dei linfonodi). Vi sono numerose patologie che possono causare bubboni, sia infettive che non, devono essere pertanto escluse le diverse cause di origine virale, fungina, neoplastica, come l'assunzione di particolari farmaci (iatrogenesi), la presenza di malattie autoimmuni, una linfoadenite o una infezione da parte di batteri diversi dallo Y. pestis.[76][77] Tra le condizioni che talvolta possono occultare o essere scambiate per linfoadenopatia da peste, l'ernia inguinale incarcerata, se è presente insieme a febbre, i granulomi venerei o la sifilide, o patologie addominali acute. Per i bubboni in prossimità del collo o ascellari, linfoadeniti da streptococco o stafilococco, malattia da graffio di gatto, tularemia. Con bubbone piccolo o quasi assente, anche febbre tifoide o infezioni da altri batteri vanno considerate.[78] In ogni caso, la peste bubbonica si differenzia da tutte le altre condizioni che comportano la formazione dei "bubboni" per via della rapida insorgenza di una febbre elevata e della fulminea progressione dell'infiammazione e del deterioramento delle condizioni generali del paziente.[40]
Per quanto riguarda la forma polmonare, la diagnosi differenziale deve essere fatta con altre patologie che comportino febbre ed emottisi, come la bronchite di origine virale, tutte le varianti della polmonite, la tubercolosi, l'embolia polmonare, le diverse infiammazioni e i tumori del polmone.[79] Tuttavia, come nel caso della forma polmonare, la rapida insorgenza dei sintomi e la gravità di essi, nonché la presenza di bubboni, indicano fortemente la peste rispetto ad altre cause.[80]
La forma setticemica è probabilmente quella che può essere confusa maggiormente con altre condizioni per via dei numerosi segni e sintomi in comune con altre patologie, come la febbre e l'ipotensione, che possono suggerire altre cause infiammatorie o infettive, nonché qualsiasi origine dello shock.[40][81]
Trattamento modifica
Per via della rapida evoluzione della malattia, il trattamento più efficace per la peste consiste in una precoce somministrazione di una terapia antibiotica per oltre dieci giorni; anche quando non vi è una diagnosi certa è consigliabile iniziare la terapia anche solo con il sospetto clinico. Di elezione si utilizza streptomicina o cloramfenicolo o combinazioni di tetraciclina e sulfamidici. Sebbene il cloramfenicolo sia altamente efficace, è considerato un farmaco di riserva per via dei suoi effetti collaterali. Tra le nuove generazioni di antibiotici, la gentamicina e la doxiciclina si sono dimostrati efficaci nel trattamento monoterapico della malattia. Infine, gli antibiotici doxiciclina e ciprofloxacina possono essere considerati anche farmaci utili per la profilassi se somministrati per un periodo di sette giorni.[82][83] Importante è l'isolamento dei malati per evitare ulteriori contagi.
Vi è la possibilità che il batterio della peste possa sviluppare una resistenza ai farmaci e diventare così nuovamente una grave minaccia per la salute delle popolazioni. Nel 1995 è stato trovato in Madagascar un caso di una forma di batterio resistente[84] mentre, nello stesso Paese, sono state segnalate ulteriori epidemie nel novembre 2014[85] e nell'ottobre 2017.[86] Basandosi su studi in vivo su animali e in vitro, la statunitense Food and Drug Administration agli inizi del XXI secolo ha approvato anche la levofloxacina come antibiotico per i pazienti con peste.[40][87]
Oltre alla somministrazione di antibiotici, il trattamento della peste prevede anche una terapia di supporto per la gestione dei sintomi più gravi, come l'eventuale verificarsi di uno stato di shock. Nonostante non siano utilizzati abitualmente, sono state proposte diverse terapie complementari, come l'immunoterapia, la terapia fagica, la terapia con batteriocine e il ricorso agli inibitori del fattore di virulenza.[3][41] Sono, inoltre, in fase di sviluppo degli inibitori in grado di bloccare nello Y. pestis un enzima che svolge un ruolo importante nella costruzione della membrana protettiva cellulare, senza la quale il batterio non può sopravvivere.[88]
Considerata l'elevata preoccupazione per un'eventuale diffusione della malattia a seguito di bioterrorismo, sono stati approntati vaccini antipestosi per prevenire l'infezione da Y. pestis, sebbene nessuno di questi sia ampiamente utilizzato a causa di dubbi sulla reale efficacia.[58] Inoltre, per via della brevità del loro effetto, vengono generalmente somministrati solo in casi di rischio evidente e programmabile di contagio, come per esempio per le figure professionali di biologi e ricercatori a contatto con il batterio.[89] Nel primo decennio del XXI secolo erano in produzione ben 17 vaccini antipestosi.[40][90] Nel caso si verificasse un'epidemia su larga scala o un attacco bioterroristico, le linee guida consigliano l'assunzione per gli eventuali contagiati, sia adulti sia bambini, di doxiciclina, somministrata per os, e ciprofloxacina o, in alternativa, il solo cloramfenicolo per gli adulti e in combinazione con la ciprofloxacina per i bambini.[3]
Prognosi modifica
Se non trattata adeguatamente, la peste in forma bubbonica porta alla morte in circa il 40-50% dei casi, mentre per quanto riguarda la forma polmonare o setticemica il decesso avviene praticamente nella quasi totalità dei pazienti. Si deve notare che gli esiti fatali di peste bubbonica sono generalmente preceduti dall'evoluzione verso una delle due forme più gravi. Se il corretto trattamento antibiotico viene attuato precocemente, vale a dire entro circa 24 ore dalla prima manifestazione dei sintomi[37], la mortalità scende fino al 5% per la forma bubbonica e al 10% per quella polmonare.[78] Nei decenni 1984-2004 vi sono stati tra i mille e i cinquemila casi diagnosticati ogni anno nel mondo, con un numero di decessi compreso tra i 100 e i 200 l'anno.[3] I casi di guarigione da peste setticemica possono essere accompagnati da lesioni permanenti ad aree periferiche colpite da necrosi, un esito frequente se il quadro di CID non viene trattato anch'esso tempestivamente, il che può portare a necessità di amputazione di dita od estremità.
Complicanze modifica
Nonostante la precoce somministrazione di un corretto trattamento possa essere risolutiva, un paziente può incorrere in una serie di potenziali complicazioni in grado di metterne a repentaglio la sopravvivenza. Tra le più significative vi è la faringite, lo sviluppo di una peste polmonare secondaria a una bubbonica, l'instaurarsi di una batteriemia o di uno shock settico. Un'ulteriore complicanza in grado di aumentare la mortalità è la meningite che può verificarsi dopo almeno una settimana dallo sviluppo di una peste bubbonica non trattata.[72][80]
Prevenzione modifica
Poiché la peste umana è una malattia rara nella maggior parte del mondo, non si ritiene necessaria la vaccinazione di routine se non per i soggetti con un rischio particolarmente elevato di esposizione al batterio. Non è nemmeno consigliato tra coloro che vivono in aree con peste enzootica, dove i casi di infezione si verificano a tassi regolari e prevedibili in particolari zone e popolazioni, come avviene negli Stati Uniti occidentali, né è indicato per la maggior parte dei viaggiatori che si recano in Paesi in cui sono stati segnalati recenti casi, in particolare se il loro viaggio è limitato alle aree urbane ed è previsto che soggiornino in strutture moderne. I centri per la prevenzione e il controllo delle malattie statunitensi raccomandano la vaccinazione per: (1) tutto il personale di laboratorio e di campo che lavora con gli organismi Y. pestis resistenti agli antimicrobici; (2) per le persone impegnate in esperimenti di aerosol con lo Y. pestis; (3) per le persone impegnate in operazioni sul campo in aree con peste enzootica in cui non è possibile prevenire l'esposizione (come alcune aree colpite da una catastrofe).[89]
Una revisione sistematica della Cochrane Collaboration non ha trovato studi di qualità sufficiente per stilare alcuna dichiarazione sull'efficacia del vaccino.[91]
Prospettive modifica
Sebbene la peste non sia una malattia comune nel XXI secolo, è comunque una patologia che non deve essere sottovalutata, per via della sua alta trasmissibilità, del rapido decorso clinico e dell'elevata mortalità. Anche un piccolo focolaio relativamente circoscritto può portare a conseguenze gravi, come accadde nel 1994 in India quando una ristretta epidemia causò cinquanta morti nella città di Surat e comportò una perdita per la nazione di circa 600 milioni di dollari a causa delle ripercussioni sul turismo e sul commercio.[92] Tuttavia, siccome è impossibile debellare la malattia e poiché essa è ampiamente diffusa nei roditori selvatici, si ritiene che sia necessario approfondire e monitorare i rischi per la popolazione umana. Ad esempio, è risaputo che climi caldi favoriscono il diffondersi del batterio e pertanto il riscaldamento globale potrebbe rappresentare un pericolo per il futuro.[93]
Il punto fondamentale per il contenimento di un focolaio è rappresentato dalla possibilità di effettuare una rapida diagnosi anche in condizioni di mancanza di strutture sanitarie all'avanguardia. Da questo punto di vista vi sono stati grandi progressi grazie all'introduzione di test diagnostici semplici e veloci, ma si mette in rilievo la necessità di introdurre ulteriori miglioramenti.[37]
Un altro grave timore per la salute umana è rappresentato dalla possibilità del generarsi di ceppi di Y. pestis resistenti agli antibiotici. Infine il pericolo che il batterio della peste possa essere utilizzato come arma biologica in attività militari o di bioterrorismo è una concreta possibilità che molti governi o autorità sanitarie prendono in seria considerazione.[37]
La peste come arma biologica modifica
La peste ha una lunga storia come arma biologica. Alcuni resoconti storici risalenti all'antica Cina e all'Europa medievale descrivono in dettaglio l'uso di carcasse di animali o cadaveri di uomini infetti da parte degli Xiongnu, degli Unni, dei Mongoli, dei Turchi e di altri popoli, per contaminare le riserve d'acqua nemiche. Si dice che il generale Huo Qubing, della dinastia Han, sia morto a causa di ciò mentre era impegnato in una guerra contro gli Xiongnu. È stato anche riportato che siano state lanciate le vittime della peste tramite catapulte all'interno di città sotto assedio con lo scopo di propagare il contagio.[94]
Nel 1347 la città di Caffa, un grande emporio commerciale nella penisola di Crimea in mano ai Genovesi, fu assediata da un esercito di guerrieri mongoli dell'Orda d'oro sotto il comando di Ganī Bek. Alcune fonti riportano che gli assedianti, logorati dalla malattia che li flagellava, presero la decisione di usare i cadaveri infetti dei propri compagni come arma biologica catapultandoli all'interno della città contagiando gli abitanti. Questo evento, forse, potrebbe essere il responsabile del propagarsi della peste nera in Europa giunta per mezzo delle navi che lasciarono Caffa.[95]
Durante la seconda guerra mondiale, l'esercito giapponese sviluppò un'arma basata sull'allevamento e il rilascio di un gran numero di pulci che potevano essere infettate dallo Y. pestis. Durante l'occupazione giapponese della Manciuria, l'Unità 731 infettò deliberatamente civili e prigionieri di guerra cinesi, coreani e abitanti della Manciuria con il batterio della peste. Questi soggetti, chiamati "maruta" vennero dissezionati per studi mentre altri vivisezionati quando erano ancora coscienti. Alcuni membri dell'unità, come Shirō Ishii furono esonerati dal comparire nel processo di Tokyo ma dodici di loro furono giudicati per crimini di guerra dal tribunale di Chabarovsk nel 1949, quando alcuni di loro ammisero di aver diffuso la peste bubbonica in un raggio di 36 km intorno alla città di Changde.[96]
Per tutta la durata della guerra fredda le grandi potenze militari hanno condotti studi per l'utilizzo della peste come arma e sui metodi di difesa nel caso che la utilizzasse un Paese nemico contro di loro. A partire dai primi anni del XXI secolo, con l'alleviarsi delle tensioni internazionali ma con la crescita delle preoccupazioni riguardanti il terrorismo, ha preso spazio il timore che lo Y. pestis possa essere utilizzato a questo scopo; infatti, se il batterio fosse rilasciato in aerosol in uno spazio ristretto e densamente abitato potrebbe causare un numero di vittime significativo e scatenare panico tra la popolazione.[97][98] Proprio per mitigare gli effetti di una tale azione di bioterrorismo molti paesi, ed in particolare gli Stati Uniti d'America, sono in possesso di grandi scorte di antibiotici.[99]
La peste nell'arte e nella letteratura modifica
A causa della sua virulenza, della paura che essa ha suscitato nel corso dei secoli e dell'enorme numero di vittime causate, molti scrittori hanno inserito un'epidemia di peste nelle loro opere, oppure hanno scritto un saggio in cui si parla della malattia o in cui essa è comunque presente.
Tra le molte opere celebri nelle quali si tratta anche della peste o di un'epidemia ad essa associabile si possono certamente ricordare:
- il Libro dei Maccabei (la peste inviata da Dio contro i Filistei);
- l'Iliade (I, 9ss.), la peste inviata per punizione da Apollo nel campo dei Greci;
- le Storie (II, 47 - 54) dello storico greco Tucidide con la peste ad Atene nell'età di Pericle;
- l'opera dello storico Diodoro Siculo (XIV, 4 - 71);
- il De rerum natura (VI 1138 - 1286) del poeta latino Lucrezio sulla peste di Atene, già descritta dallo storico greco
Tucidide nella Guerra del Peloponneso;
- il brano sulla peste del Norico (libro IV, vv. 453-527) nelle Georgiche di Virgilio;
- Le metamorfosi (VII 523 - 613) del poeta latino Ovidio;
- le Storie (XIX 4, 4) dello storico romano Ammiano Marcellino;
- la Guerra persiana (II 22 - 23) dello storico medievale Procopio di Cesarea nel VI secolo d. C.;
- la Historia Langobardorum di Paolo Diacono (II, 4) che descrive la peste scoppiata in Italia (VI sec. d.C.) al tempo di Giustiniano;
- il Decameron di Giovanni Boccaccio (novelle scritte nel 1349-1351 circa);
- il Diario dell'anno della peste di Daniel Defoe (1722);
- la Storia della colonna infame (saggio storico, 1840) e I promessi sposi (romanzo storico, 1840; capitoli XXXI e XXXII) entrambi di Alessandro Manzoni;
- La maschera della morte rossa di Edgar Allan Poe (1842);
- Il barbiere di sua altezza di Luigi Gramegna, romanzo storico che descrive l'epidemia torinese del 1630;
- La peste (1947) e Lo stato d'assedio (1948) di Albert Camus. L'opera di quest'ultimo ha una valenza allegorica: la peste rappresenta i regimi totalitari, in particolare la diffusione del nazismo in Europa;
- molte opere contemporanee di fantascienza contenenti il motivo di un virus pestifero che si diffonde seminando morte fra le popolazioni. Tra le varie opere si ricorda L'ombra dello scorpione di Stephen King (1978; 1990).
La pittura tardo medievale ebbe ripercussioni dalle tragedie legate alla pestilenza. La cosiddetta "danza macabra", uno dei temi iconografici più frequenti dei primi decenni del XV secolo nella quale è rappresentata una danza tra uomini e scheletri, è stata messa in relazione con la peste del Trecento. Una delle produzioni più celebri è la Danza macabra di Lubecca, opera del pittore e intagliatore Bernt Notke, andata perduta a seguito del Bombardamento di Lubecca.[100][101] Tale tema venne utilizzato anche per le musiche di Totentanz, composte tra il 1834 e il 1859 da Franz Liszt. Il pittore tedesco del XX secolo Werner Tübke ricorse al soggetto della peste per una scena del suo monumentale dipinto dedicato alla guerra dei contadini tedeschi del XVI secolo.[102][103]
Note modifica
- ^ Regolamento sanitario internazionale, su salute.gov.it. URL consultato il 2 febbraio 2018 (archiviato il 3 febbraio 2018).
- ^ (EN) Plague, su World Health Organization. URL consultato il 4 novembre 2017 (archiviato il 24 aprile 2015).
- ^ a b c d e f g h i j k l m n o p q Yang R, Plague: Recognition, Treatment, and Prevention, in J. Clin. Microbiol., vol. 56, n. 1, gennaio 2018, DOI:10.1128/JCM.01519-17, PMC 5744195, PMID 29070654.
- ^ a b Doyle TM, Matuschak GM, Lechner AJ, Septic shock and nonpulmonary organ dysfunction in pneumonic plague: the role of Yersinia pestis pCD1- vs. pgm- virulence factors, in Crit. Care Med., vol. 38, n. 7, luglio 2010, pp. 1574-83, DOI:10.1097/CCM.0b013e3181de8ace, PMID 20400901.
- ^ a b Raoult D, Mouffok N, Bitam I, Piarroux R, Drancourt M, Plague: history and contemporary analysis, in J. Infect., vol. 66, n. 1, gennaio 2013, pp. 18-26, DOI:10.1016/j.jinf.2012.09.010, PMID 23041039.
- ^ Cosmacini, p. 6.
- ^ Pèste, in Treccani.it – Vocabolario Treccani on line, Roma, Istituto dell'Enciclopedia Italiana.
- ^ Naphy e Spicer, pp. 29-30.
- ^ Zuchora-Walske, p. 53.
- ^ Montanari, Massimo, Storia medievale, 23ª ed., Laterza, 2006, pp. 243-244, ISBN 978-88-420-6540-1.
- ^ The last years of Justinian I - Byzantyne Empire -, su Encyclopedia Britannica.
- ^ Mark Welford, Geographies of Plague Pandemics: The Spatial-Temporal Behavior of Plague to the Modern Day, Routledge, 9 apr. 2018, ISBN 9781315307435.«In many respects, the medieval black Death killed off the feudal, restrictive and medieval society, with its serfs and protected guilds, and gave birth to our own industrialized consumer society (...)»
- ^ Gomme A. W., Andrewes A., Dover, K. J., An Historical Commentary on Thucydides, vol. 5, Oxford University Press, 1981, Book VIII.
- ^ Naphy e Spicer, p. 10.
- ^ Ujvari, pp. 35-36.
- ^ Ujvari, p. 45.
- ^ Naphy e Spicer, p. 13.
- ^ Naphy e Spicer, pp. 16-17.
- ^ Frari, pp. 296-297.
- ^ Frari, p. 298.
- ^ Alchon, p. 21.
- ^ Historical Estimates of World Population, su census.gov. URL consultato il 27 settembre 2018 (archiviato dall'url originale il 9 luglio 2012).
- ^ Naphy e Spicer, p. 67.
- ^ a b Naphy e Spicer, p. 69.
- ^ Naphy e Spicer, p. 71.
- ^ a b Naphy e Spicer, p. 70.
- ^ Naphy e Spicer, p. 85.
- ^ Naphy e Spicer, p. 95.
- ^ Naphy e Spicer, pp. 90, 94.
- ^ Naphy e Spicer, pp. 111-112.
- ^ Putzker M, Sauer H, Sobe D, Plague and other human infections caused by Yersinia species, in Clin. Lab., vol. 47, n. 9-10, 2001, pp. 453-66, PMID 11596907.
- ^ a b c d e f Perry RD, Fetherston JD, Yersinia pestis--etiologic agent of plague, in Clin. Microbiol. Rev., vol. 10, n. 1, gennaio 1997, pp. 35-66, PMC 172914, PMID 8993858.
- ^ a b c Christakos, pp. 110-114.
- ^ Cosmacini, p. 19.
- ^ a b c Plague, su World Health Organization, ottobre 2017. URL consultato l'8 novembre 2017 (archiviato il 24 aprile 2015).
- ^ Schrag SJ, Wiener P, Emerging infectious disease: what are the relative roles of ecology and evolution?, in Trends Ecol. Evol. (Amst.), vol. 10, n. 8, agosto 1995, pp. 319-24, DOI:10.1016/s0169-5347(00)89118-1, PMID 21237055.
- ^ a b c d e f g h i Stenseth NC, Atshabar BB, Begon M, Belmain SR, Bertherat E, Carniel E, Gage KL, Leirs H, Rahalison L, Plague: past, present, and future, in PLoS Med., vol. 5, n. 1, gennaio 2008, pp. e3, DOI:10.1371/journal.pmed.0050003, PMC 2194748, PMID 18198939.
- ^ (EN) Plague. Disease outbreak news, su who.int. URL consultato il 12 dicembre 2019 (archiviato il 25 giugno 2012).
- ^ (FR) Bertherat E, Lamine KM, Formenty P, Thuier P, Mondonge V, Mitifu A, Rahalison L, Major pulmonary plague outbreak in a mining camp in the Democratic Republic of Congo: brutal awakening of an old scourge, in Med Trop (Mars), vol. 65, n. 6, novembre 2005, pp. 511-4, PMID 16555508.
- ^ a b c d e f g h i j k Dillard RL, Juergens AL, Plague, 019 Jan–. 2019 Oct 27, PMID 31751045.
- ^ a b c Anisimov AP, Amoako KK, Treatment of plague: promising alternatives to antibiotics, in J. Med. Microbiol., vol. 55, Pt 11, novembre 2006, pp. 1461-75, DOI:10.1099/jmm.0.46697-0, PMID 17030904.
- ^ Cui Y, Yu C, Yan Y, Li D, Li Y, Jombart T, Weinert LA, Wang Z, Guo Z, Xu L, Zhang Y, Zheng H, Qin N, Xiao X, Wu M, Wang X, Zhou D, Qi Z, Du Z, Wu H, Yang X, Cao H, Wang H, Wang J, Yao S, Rakin A, Li Y, Falush D, Balloux F, Achtman M, Song Y, Wang J, Yang R, Historical variations in mutation rate in an epidemic pathogen, Yersinia pestis, in Proc. Natl. Acad. Sci. U.S.A., vol. 110, n. 2, gennaio 2013, pp. 577-82, DOI:10.1073/pnas.1205750110, PMC 3545753, PMID 23271803.
- ^ Zhou J, Bi Y, Xu X, Qiu Y, Wang Q, Feng N, Cui Y, Yan Y, Zhou L, Tan Y, Yang H, Du Z, Han Y, Song Y, Zhang P, Zhou D, Cheng Y, Zhou Y, Yang R, Wang X, Bioluminescent tracking of colonization and clearance dynamics of plasmid-deficient Yersinia pestis strains in a mouse model of septicemic plague, in Microbes Infect., vol. 16, n. 3, marzo 2014, pp. 214-24, DOI:10.1016/j.micinf.2013.11.013, PMID 24333143.
- ^ N. V. Popov, A. A. Sludskiĭ e A. I. Udovikov, [Role of Yersinia pestis biofilms in mechanisms of plague enzootics], in Zhurnal Mikrobiologii, Epidemiologii I Immunobiologii, n. 4, 2008-07, pp. 118–120. URL consultato il 18 aprile 2022.
- ^ Mark Welford e Brian Bossak, Body Lice, Yersinia pestis Orientalis, and Black Death, in Emerging Infectious Diseases, vol. 16, n. 10, 2010-10, pp. 1649–1651, DOI:10.3201/eid1610.100683. URL consultato il 18 aprile 2022.
- ^ Cosmacini, pp. 7-8.
- ^ A. W. Bacot, LXXXII. Notes on the development of Bacillus pestis in bugs (Cimex lectularius) and their power to convey infection, in The Journal of Hygiene, vol. 14, Suppl, 1915-01, pp. 777–792.3. URL consultato il 19 aprile 2022.
- ^ (FR) BLANC G, [Non-conforming opinion on the transmission of plague], in Rev Hyg Med Soc, vol. 4, n. 6, settembre 1956, pp. 535-62, PMID 13401156.
- ^ Mark Welford e Brian Bossak, Body Lice, Yersinia pestis Orientalis, and Black Death, in Emerging Infectious Diseases, vol. 16, n. 10, 2010-10, pp. 1649–1651, DOI:10.3201/eid1610.100683. URL consultato il 19 aprile 2022.
- ^ Linda Houhamdi, Hubert Lepidi e Michel Drancourt, Experimental model to evaluate the human body louse as a vector of plague, in The Journal of Infectious Diseases, vol. 194, n. 11, 1º dicembre 2006, pp. 1589–1596, DOI:10.1086/508995. URL consultato il 19 aprile 2022.
- ^ (EN) Coronavirus: What can the 'plague village' of Eyam teach us?, in BBC News, 22 aprile 2020. URL consultato il 19 aprile 2022.
- ^ (EN) Nils Chr. Stenseth, Yuxin Tao e Chutian Zhang, No evidence for persistent natural plague reservoirs in historical and modern Europe, in Proceedings of the National Academy of Sciences, vol. 119, n. 51, 20 dicembre 2022, pp. e2209816119, DOI:10.1073/pnas.2209816119. URL consultato il 31 gennaio 2023.
- ^ Peste Nera: non fu colpa dei ratti - Focus.it, su web.archive.org, 31 gennaio 2023. URL consultato il 31 gennaio 2023 (archiviato dall'url originale il 31 gennaio 2023).
- ^ Hinnebusch B.J., Rudolph A.E., Cherepanov P., Dixon J.E., Schwan T.G., Forsberg A., Role of Yersinia murine toxin in survival of Yersinia pestis in the midgut of the flea vector, in Science, (#5, 568), n. 296, 2002, p. 733–735, Bibcode:Bibcode:2002Sci...296..733H..
- ^ Ruth Rogaski, The Manchurian Plague and COVID-19: China, the United States, and the “Sick Man,” Then and Now, in American Journal of Public Health, vol. 111, n. 3, 2021-3, pp. 423–429, DOI:10.2105/AJPH.2020.305960. URL consultato il 19 aprile 2022.
- ^ Mark Gamsa, The Epidemic of Pneumonic Plague in Manchuria 1910-1911, in Past & Present, n. 190, 2006, pp. 147–183. URL consultato il 19 aprile 2022.
- ^ Di Giorgia, La peste nel Decameron di Boccaccio, su Archeoares, 1º aprile 2020. URL consultato il 19 aprile 2022.
- ^ a b c Butler T, Plague into the 21st century, in Clin. Infect. Dis., vol. 49, n. 5, settembre 2009, pp. 736-42, DOI:10.1086/604718, PMID 19606935.
- ^ (EN) Roger D. Pechous, Vijay Sivaraman e Paul A. Price, Early Host Cell Targets of Yersinia pestis during Primary Pneumonic Plague, in PLOS Pathogens, vol. 9, n. 10, 3 ott 2013, pp. e1003679, DOI:10.1371/journal.ppat.1003679. URL consultato il 19 aprile 2022.
- ^ Centers for Disease Control and Prevention; Plague, Symptoms, su cdc.gov. URL consultato il 26 marzo 2018 (archiviato il 15 agosto 2019).
- ^ a b c d e Ujvari, p. 64.
- ^ a b c d e Cosmacini, p. 8.
- ^ Brown S.D., Montie T.C., Beta-Adreginic Blocking activity of Yersinia Pestis Murine Toxin, in Infection and Immunity, vol. 18, n. 1, 22 marzo 1977, pp. 85-93. URL consultato il 26 marzo 2018 (archiviato dall'url originale il 16 aprile 2018).
- ^ a b CHARI MV, Pneumonic plague, in Lancet, vol. 1, n. 6506, maggio 1948, p. 728, DOI:10.1016/s0140-6736(48)90422-x, PMID 18857150.
- ^ Pechous RD, Sivaraman V, Stasulli NM, Goldman WE, Pneumonic Plague: The Darker Side of Yersinia pestis, in Trends Microbiol., vol. 24, n. 3, marzo 2016, pp. 190-197, DOI:10.1016/j.tim.2015.11.008, PMID 26698952.
- ^ Donadini R, Fields BA, Yersinia pseudotuberculosis superantigens, in Chem Immunol Allergy, vol. 93, 2007, pp. 77-91, DOI:10.1159/000100859, PMID 17369701.
- ^ Brady MF, Anjum F, Yersinia Pseudotuberculosis, PMID 28613468.
- ^ Fàbrega A, Vila J, Yersinia enterocolitica: pathogenesis, virulence and antimicrobial resistance, in Enferm. Infecc. Microbiol. Clin., vol. 30, n. 1, gennaio 2012, pp. 24-32, DOI:10.1016/j.eimc.2011.07.017, PMID 22019131.
- ^ a b Chanteau S., Rahalison L., Ralafiarisoa L., Foulon J., Ratsitorahina M., Ratsifasoamanana L., Carniel E. e Nato F., Development and testing of a rapid diagnostic test for bubonic and pneumonic plague, in Lancet, vol. 361, n. 9353, gennaio 2003, pp. 211-6, DOI:10.1016/S0140-6736(03)12270-2, PMID 12547544.
- ^ Reed WP, Palmer DL, Williams RC, Kisch AL, Bubonic plague in the Southwestern United States. A review of recent experience, in Medicine (Baltimore), vol. 49, n. 6, novembre 1970, pp. 465-86, DOI:10.1097/00005792-197011000-00002, PMID 4924535.
- ^ Gage KL, Dennis DT, Orloski KA, Ettestad P, Brown TL, Reynolds PJ, Pape WJ, Fritz CL, Carter LG, Stein JD, Cases of cat-associated human plague in the Western US, 1977-1998, in Clin. Infect. Dis., vol. 30, n. 6, giugno 2000, pp. 893-900, DOI:10.1086/313804, PMID 10852811.
- ^ a b Prentice MB, Rahalison L, Plague, in Lancet, vol. 369, n. 9568, aprile 2007, pp. 1196-207, DOI:10.1016/S0140-6736(07)60566-2, PMID 17416264.
- ^ Rollins SE, Rollins SM, Ryan ET, Yersinia pestis and the plague, in Am. J. Clin. Pathol., 119 Suppl, giugno 2003, pp. S78–85, DOI:10.1309/DQM9-3R8Q-NQWB-FYU8, PMID 12951845.
- ^ Qu S, Shi Q, Zhou L, Guo Z, Zhou D, Zhai J, Yang R, Ambient stable quantitative PCR reagents for the detection of Yersinia pestis, in PLoS Negl Trop Dis, vol. 4, n. 3, marzo 2010, pp. e629, DOI:10.1371/journal.pntd.0000629, PMC 2834737, PMID 20231881.
- ^ Mölsä M, Hemmilä H, Katz A, Niemimaa J, Forbes KM, Huitu O, Stuart P, Henttonen H, Nikkari S, Monitoring biothreat agents (Francisella tularensis, Bacillus anthracis and Yersinia pestis) with a portable real-time PCR instrument, in J. Microbiol. Methods, vol. 115, agosto 2015, pp. 89-93, DOI:10.1016/j.mimet.2015.05.026, PMID 26043838.
- ^ Earwood JS, Thompson TD, Hemoptysis: evaluation and management, in Am Fam Physician, vol. 91, n. 4, febbraio 2015, pp. 243-9, PMID 25955625.
- ^ Vincent JL, De Backer D, Circulatory shock, in N. Engl. J. Med., vol. 369, n. 18, ottobre 2013, pp. 1726-34, DOI:10.1056/NEJMra1208943, PMID 24171518.
- ^ a b Eugene Braunwald e Tinsley Randolph Harrison, Harrison's principles of internal medicine, 11th ed, McGraw-Hill, 1988, p. 616, ISBN 0-07-007261-2, OCLC 847293372. URL consultato il 22 dicembre 2021.
- ^ Kugeler KJ, Apangu T, Forrester JD, Griffith KS, Candini G, Abaru J, Okoth JF, Apio H, Ezama G, Okello R, Brett M, Mead P, Knowledge and practices related to plague in an endemic area of Uganda, in Int. J. Infect. Dis., vol. 64, novembre 2017, pp. 80-84, DOI:10.1016/j.ijid.2017.09.007, PMID 28935246.
- ^ a b Andrianaivoarimanana V, Piola P, Wagner DM, Rakotomanana F, Maheriniaina V, Andrianalimanana S, Chanteau S, Rahalison L, Ratsitorahina M, Rajerison M, Trends of Human Plague, Madagascar, 1998-2016, in Emerging Infect. Dis., vol. 25, n. 2, febbraio 2019, pp. 220-228, DOI:10.3201/eid2502.171974, PMC 6346457, PMID 30666930.
- ^ Adams DA, Thomas KR, Jajosky RA, Foster L, Baroi G, Sharp P, Onweh DH, Schley AW, Anderson WJ, Summary of Notifiable Infectious Diseases and Conditions - United States, 2015, in MMWR Morb. Mortal. Wkly. Rep., vol. 64, n. 53, agosto 2017, pp. 1-143, DOI:10.15585/mmwr.mm6453a1, PMID 28796757.
- ^ Mwengee W, Thomas Butler, Samuel Mgema, George Mhina, Yusuf Almasi, Charles Bradley, James B. Formanik e C. George Rochester, Treatment of Plague with Genamicin or Doxycycline in a Randomized Clinical Trial in Tanzania, in Clin Infect Dis, vol. 42, n. 5, 2006, pp. 614-21, DOI:10.1086/500137, PMID 16447105.
- ^ Marianne Abele-Horn: Antimikrobielle Therapie. Entscheidungshilfen zur Behandlung und Prophylaxe von Infektionskrankheiten. Unter Mitarbeit von Werner Heinz, Hartwig Klinker, Johann Schurz und August Stich, 2., überarbeitete und erweiterte Auflage. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4, S. 159.
- ^ Drug-resistant plague a 'major threat', say scientists Archiviato il 19 luglio 2012 in Internet Archive., SciDev.Net.
- ^ Plague – Madagascar, su who.int, World Health Organisation, 21 novembre 2014. URL consultato il 26 novembre 2014 (archiviato il 3 gennaio 2016).
- ^ WHO scales up response to plague in Madagascar, su who.int, World Health Organization (WHO), 1º ottobre 2017. URL consultato il 5 ottobre 2017 (archiviato il 23 aprile 2018).
- ^ Gosche JR, Vick L, Acute, subacute, and chronic cervical lymphadenitis in children, in Semin. Pediatr. Surg., vol. 15, n. 2, maggio 2006, pp. 99-106, DOI:10.1053/j.sempedsurg.2006.02.007, PMID 16616313.
- ^ Hirschbeck MW, Kuper J, Lu H, Liu N, Neckles C, Shah S, Wagner S, Sotriffer CA, Tonge PJ, Kisker C, Structure of the Yersinia pestis FabV enoyl-ACP reductase and its interaction with two 2-pyridone inhibitors, in Structure, vol. 20, n. 1, gennaio 2012, pp. 89-100, DOI:10.1016/j.str.2011.07.019, PMC 3361726, PMID 22244758.
- ^ a b Plague Vaccine, su cdc.gov, CDC, 11 giugno 1982. URL consultato il 30 aprile 2015 (archiviato il 14 luglio 2018).
- ^ Ferrer R, Lymphadenopathy: differential diagnosis and evaluation, in Am Fam Physician, vol. 58, n. 6, ottobre 1998, pp. 1313-20, PMID 9803196.
- ^ Jefferson T, Demicheli V, Pratt M, Demicheli e Pratt, Vaccines for preventing plague, in Tom Jefferson (a cura di), Cochrane Database Syst Rev, n. 2, 2000, pp. CD000976, DOI:10.1002/14651858.CD000976, PMC 6532692, PMID 10796565.
- ^ Fritz CL, Dennis DT, Tipple MA, Campbell GL, McCance CR, Gubler DJ, Surveillance for pneumonic plague in the United States during an international emergency: a model for control of imported emerging diseases, in Emerging Infect. Dis., vol. 2, n. 1, 1996, pp. 30-6, DOI:10.3201/eid0201.960103, PMC 2639812, PMID 8964057.
- ^ Mudur G, India's pneumonic plague outbreak continues to baffle, in BMJ, vol. 311, n. 7007, settembre 1995, p. 706, DOI:10.1136/bmj.311.7007.706a, PMC 2550762, PMID 7549679.
- ^ Schama, S. (2000). A History of Britain: At the Edge of the World? 3000BC–AD1603, First Edition, BBC Worldwide, London, p226.
- ^ Wheelis M., Biological warfare at the 1346 siege of Caffa, in Emerg Infect Dis, vol. 8, n. 9, 2002, pp. 971-75, DOI:10.3201/eid0809.010536, PMC 2732530, PMID 12194776. URL consultato il 13 dicembre 2019 (archiviato il 4 settembre 2011).
- ^ Barenblatt, 2004, pp. 220-221.
- ^ Inglesby TV, Dennis DT, Henderson DA, Bartlett JG, Ascher MS, Eitzen E, Fine AD, Friedlander AM, Hauer J, Koerner JF, Layton M, McDade J, Osterholm MT, O'Toole T, Parker G, Perl TM, Russell PK, Schoch-Spana M, Tonat K, Plague as a biological weapon: medical and public health management. Working Group on Civilian Biodefense, in JAMA, vol. 283, n. 17, maggio 2000, pp. 2281-90, DOI:10.1001/jama.283.17.2281, PMID 10807389.
- ^ Koirala J, Plague: disease, management, and recognition of act of terrorism, in Infect. Dis. Clin. North Am., vol. 20, n. 2, giugno 2006, pp. 273–87, viii, DOI:10.1016/j.idc.2006.02.004, PMID 16762739.
- ^ Tamparo e Lewis, 2011, p. 70.
- ^ Peste, in Enciclopedia Italiana, Roma, Istituto dell'Enciclopedia Italiana.
- ^ (EN) Lübeck's Dance of Death, su dodedans.com. URL consultato il 28 settembre 2012 (archiviato dall'url originale il 10 luglio 2012).
- ^ Seigneuret, p. 326.
- ^ Gaehtgens e Zelljadt, p. 109.
Bibliografia modifica
- (EN) Suzanne Austin Alchon, A pest in the land: new world epidemics in a global perspective, 1ª ed, University of New Mexico Press, 2003, ISBN 0-8263-2870-9, OCLC 50773314. URL consultato il 27 settembre 2018.
- (EN) Daniel Barenblatt, A Plague upon Humanity: The Secret Genocide of Axis Japan's Germ Warfare Operation, HarperCollins, 2004, ISBN 978-0-06-018625-8.
- Giorgio Cosmacini, Storia della medicina e della sanità in Italia : dalla peste nera ai giorni nostri, 1. ed, Bari, Laterza, 2005, ISBN 88-420-7767-4, OCLC 62362855.
- Angelo Antonio Frari, Secolo XIV, in Della peste e della publica administrazione sanitaria, Venezia, Tipografia di Francesco Andreola, 1840, pp. 296 e segg, ISBN non esistente.
- Anna Foa, Ebrei in Europa: dalla peste nera all'emancipazione XIV-XVIII secolo, Laterza, 1992, ISBN 88-420-3947-0, OCLC 27071770.
- (EN) Thomas Gaehtgens e Katja Zelljadt (a cura di), Getty Research Journal, Volume 3, Getty Publications, 2011, ISBN 978-1-60606-063-6.
- Massimo Montanari, Storia medievale, 23ª ed., editori Laterza, 2006, ISBN 978-88-420-6540-1.
- William Naphy e Andrew Spicer, La peste in Europa, Il Mulino, 2006, ISBN 978-88-15-10967-5, OCLC 68598883.
- Stefan Cunha Ujvari, Storia delle epidemie, Bologna, Odoya, 2002, ISBN 978-88-6288-127-2, OCLC 775569586.
- (EN) Carol Tamparo e Marcia Lewis, Diseases of the Human Body, Filadelfia, F.A. Davis Company, 2011, ISBN 978-0-8036-2505-1.
- (EN) Jean-Charles Seigneuret, Dictionary of Literary Themes and Motifs, a cura di Peter Lee, Volume 1, Greenwood Publishing Group, 1988, ISBN 978-0-313-22943-5.
- (EN) Christine Zuchora-Walske, Poland. Countries of the World, ABDO, 2013, ISBN 978-1-61783-634-3.
Voci correlate modifica
Altri progetti modifica
- Wikiquote contiene citazioni sulla peste
- Wikizionario contiene il lemma di dizionario «peste»
- Wikimedia Commons contiene immagini o altri file sulla peste
Collegamenti esterni modifica
- peste, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- Aldo Castellani, Filippo Rho, Nino Baboni, PESTE, in Enciclopedia Italiana, Istituto dell'Enciclopedia Italiana, 1935.
- peste, in Dizionario di storia, Istituto dell'Enciclopedia Italiana, 2010.
- (IT, DE, FR) Peste, su hls-dhs-dss.ch, Dizionario storico della Svizzera.
- (EN) plague, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN) Opere riguardanti Peste, su Open Library, Internet Archive.
| Controllo di autorità | Thesaurus BNCF 8342 · LCCN (EN) sh85102591 · GND (DE) 4045326-1 · BNF (FR) cb11933083q (data) · J9U (EN, HE) 987007550799105171 · NDL (EN, JA) 00569104 |
|---|
| Classificazione e risorse esterne (EN) |
ICD-9-CM: 020.9 e 020; ICD-10: A20; ICD-10-CM: A20 e A20.9; MeSH: D010930; DiseasesDB: 14226; |